LM11A-31 药物在试验中延缓了阿尔茨海默病的进展
最近審查:02.07.2025

在最近发表在《自然医学》杂志上的一项研究中,科学家进行了一项随机、双盲、安慰剂对照的 2a 期研究,以检验 LM11A-31 通过调节 p75 神经营养因子受体 (p75NTR) 治疗阿尔茨海默病 (AD) 的安全性和有效性。
晚发型AD是最常见的痴呆症,其特征是突触功能衰竭、退化和神经细胞丢失。尽管目前两种治疗AD的主要药物靶向异常淀粉样β蛋白或tau蛋白的积累,但它们仅能解决部分病理生理机制。另一种方法是靶向影响基础生物学通路的受体和信号网络。临床前研究表明,用一种新型小分子LM11A-31调节p75NTR,可以减少淀粉样蛋白和异常tau蛋白引起的突触丢失。
研究描述
在这项随机临床试验中,研究人员检查了 LM11A-31 是否可以通过调节人类的 p75NTR 来减缓阿尔茨海默病的进展。
研究参与者以1:1:1的比例,向242名患有轻度至中度哮喘的患者服用200毫克和400毫克剂量的LM11A-31口服胶囊或安慰剂,持续26周。参与者均已通过生物学方法确诊为阿尔茨海默病(脑脊液淀粉样β蛋白42 (Aβ42) 水平低于550 ng/L或Aβ42:β40比例低于0.89),诊断符合McKhann标准,简易精神病学检查量表 (MMSE) 评分为18至26分,老年抑郁量表 (GDS) 评分低于5.0分,改良哈钦斯基缺血量表 (HIS) 评分≤4.0分,正规教育年限≥8年,且既往认知能力下降≥6个月。
符合条件的参与者在入选研究前已服用乙酰胆碱酯酶抑制剂 (AChEI) 或部分 NMDA 受体拮抗剂≥ 3 个月。他们未服用违禁药物,例如抗精神病药、苯二氮卓类药物、抗癫痫药、镇静剂、中枢活性抗高血压药、益智药(银杏除外)或含阿片类镇痛药。
研究的主要结局是安全性和耐受性,采用哥伦比亚自杀想法和行为严重程度评定量表 (C-SSRS)、生命体征、血压和血液学参数进行评估。结构磁共振成像 (cMRI)、氟脱氧葡萄糖正电子发射断层扫描 (FDG-PET) 和脑脊液 (CSF) 生物标志物用于评估次要认知结局。AD 指标包括苏氨酸 181 磷酸化 tau、总 tau 蛋白、Aβ40、Aβ42 和乙酰胆碱酯酶 (AChE) 活性。研究团队使用定制的神经心理学测试在基线、第 12 周和第 26 周评估次要认知结局。
研究成果
研究发现LM11A-31安全性高,耐受性良好,无显著安全隐患。最常见的不良事件包括头痛、腹泻、嗜酸性粒细胞增多和鼻咽炎,其中胃肠道问题和嗜酸性粒细胞增多是停药的主要原因。400毫克组的停药人数高于200毫克组和安慰剂组。MRI检查未发现任何安全隐患,包括淀粉样蛋白相关异常。两组患者的认知评分和淀粉样蛋白异常均无显著差异。
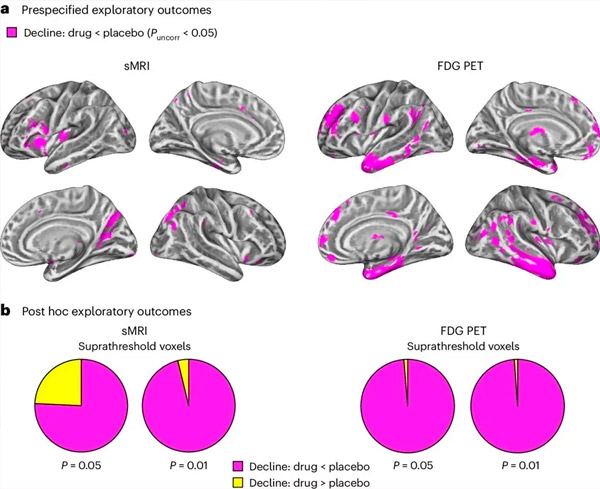
A. 双向混合模型协方差分析检验了治疗(药物或安慰剂)与时间(治疗前或治疗后)之间的相互作用。单尾t对比检验了相互作用假设(与安慰剂相比,药物可减缓病情进展),结果显示,与安慰剂组(cMRI,n = 66;PET,n = 62)相比,LM11A-31 治疗在药物组(cMRI,n = 127;PET,n = 121)中减缓了纵向退化(左图)和葡萄糖代谢减慢(右图)。显示这种相互作用的体素在人群特定皮层表面上以未校正的 P < 0.05 阈值(洋红色)显示。左半球和右半球分别显示在上行和下行。显示与假设不一致相互作用的脑区显示在补充资料中的图 7 中。
B. 在每种成像方式(cMRI,左图;FDG PET,右图)中,预先定义的易受攻击的AD脑区中体素总数(饼图总面积)显示,在未校正P < 0.01和P < 0.05的阈值越来越宽松的情况下,与假设相符(洋红色)或与假设不一致(黄色)的相互作用。蒙特卡洛模拟显示,与基于随机生成的cMRI和PET数据观察到的效应相符与与假设不一致的体素比例显著高于(每种方式的P < 0.001;双尾检验)。
与安慰剂组相比,LM11A-31 有效降低了脑脊液 Aβ42 和 Aβ40 的增幅。该药物还显示突触前蛋白生物标志物 SNAP25 的年平均百分比变化降低,突触后生物标志物 NG 的年平均百分比变化降低,表明突触前和突触后连接的丢失减缓。LM11A-31 还降低了 YKL40 的增幅,导致 MMSE 评分下降,ADAS-Cog-13 评分上升。该药物还减少了额叶和后顶叶皮质的灰质损失,并降低了内嗅皮质、颞叶皮质、海马、岛叶皮质和前额叶皮质等区域的葡萄糖代谢。
结论
研究得出结论,LM11A-31 对 p75NTR 的调节适合更大规模的临床试验。LM11A-31 达到了主要安全性终点,并且在轻度至重度 AD 患者中耐受性良好。结果表明,需要开展更长期的进一步研究,以评估小分子调节 p75NTR 作为 AD 疾病修饰疗法的潜力。研究表明,LM11A-31 显著影响了多种生物标志物,包括 Aβ40、Aβ42、SNAP25、NG 和 YKL40,表明病理进展减缓。未来的研究可能会评估其他神经胶质细胞健康指标。

