甲状旁腺
該文的醫學專家
最近審查:04.07.2025

1879年,瑞典科学家S. Sandstrom描述了人类的甲状旁腺,并为其命名。甲状旁腺是人体的重要器官,其功能是产生和分泌甲状旁腺激素(PTH),这是钙磷代谢的主要调节剂之一。
上甲状旁腺(glandula parathyma superior)和下甲状旁腺(glandula parathyma inferior)是一对圆形或卵圆形体,位于甲状腺每个叶的背面:一个位于顶部,另一个位于底部。每个腺体长4-8毫米,宽3-4毫米,厚2-3毫米。这些腺体的数量不固定,从2个到7-8个不等,平均有4个。腺体总质量平均为1.18克。
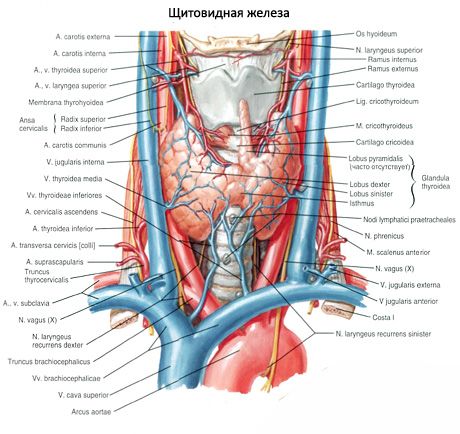
甲状旁腺与甲状腺的区别在于甲状旁腺颜色较浅(儿童为淡粉色,成人为黄褐色)。甲状旁腺通常位于甲状腺下动脉或其分支穿过甲状腺组织的部位。甲状旁腺通过其自身的纤维囊与周围组织隔开,结缔组织层由此延伸至腺体。纤维囊内含有大量血管,并将甲状旁腺划分为上皮细胞群。
腺体的实质由主甲状旁腺细胞和嗜酸性甲状旁腺细胞组成,这些细胞呈索状或簇状排列,周围环绕着细长的结缔组织纤维束。这两种细胞被认为是甲状旁腺细胞发育的不同阶段。主甲状旁腺细胞呈多面体形,胞质嗜碱性,含有大量核糖体。这些细胞中,深色(分泌活跃)和浅色(分泌较少)细胞明显不同。嗜酸性甲状旁腺细胞体积较大,轮廓清晰,含有许多带有糖原颗粒的小线粒体。
甲状旁腺激素甲状旁腺素(甲状旁腺激素)是一种蛋白质成分,参与调节磷钙代谢。甲状旁腺激素可减少尿液中钙的排泄,并在维生素D存在下增加其在肠道中的吸收。甲状腺降钙素是甲状旁腺激素的拮抗剂。
甲状旁腺的胚胎发生
甲状旁腺由成对的第三和第四鳃囊上皮发育而成。在发育的第7周,体表上皮的雏形从鳃囊壁分离,并在生长过程中向尾部移动。随后,正在形成的甲状旁腺在甲状腺左右叶的后表面上占据一个固定的位置。
 [ 7 ]、[ 8 ]、[ 9 ]、[ 10 ]、[ 11 ]、[ 12 ]
[ 7 ]、[ 8 ]、[ 9 ]、[ 10 ]、[ 11 ]、[ 12 ]
甲状旁腺的血管和神经
甲状旁腺的血液供应来自甲状腺上动脉和下动脉的分支,以及食管支和气管支。静脉血通过同名静脉流出。甲状旁腺的神经支配与甲状腺的神经支配相似。
甲状旁腺的年龄相关特征
新生儿甲状旁腺的总质量在6至9毫克之间波动。在出生后的第一年,其总质量会增加3-4倍,到5岁时再增加一倍,到10岁时增加两倍。20年后,四个甲状旁腺的总质量达到120-140毫克,并保持恒定直至老年。在所有年龄段,女性甲状旁腺的质量略大于男性。
人体通常有两对甲状旁腺(上、下),位于甲状腺背面,甲状腺囊外,靠近上下极。然而,甲状旁腺的数量和位置可能有所不同;有时甚至有多达12个甲状旁腺。它们可位于甲状腺和胸腺组织内、前纵隔和后纵隔内、心包内、食管后方、颈动脉分叉处。上甲状旁腺呈扁平卵圆形,下甲状旁腺呈球形。它们的大小约为6x3至4x1.5-3毫米,总重量为0.05至0.5克,颜色为红色或黄褐色。甲状旁腺的血液供应主要来自甲状腺下动脉的分支,静脉血流通过甲状腺静脉、食管和气管回流。甲状旁腺受喉返神经和喉上神经的交感神经纤维支配,副交感神经支配则由迷走神经进行。甲状旁腺被一层薄的结缔组织囊包裹;从囊中延伸出来的隔膜深入腺体内部。囊内含有血管和神经纤维。甲状旁腺的实质由甲状旁腺细胞或主细胞组成,根据染色程度,可区分为具有激素活性的亮细胞或亮细胞以及静息的暗细胞。主细胞形成簇、索状和簇状,老年主细胞则形成囊腔内有胶质的滤泡。在成人中,甲状旁腺主要位于其周围,呈伊红染色,被称为嗜酸性细胞或嗜酸细胞,它们是正在退化的主细胞。在甲状旁腺中,也可发现介于主细胞和嗜酸细胞之间的过渡形式。
1972 年以后,人们首次成功地阐明了甲状旁腺激素的合成问题、破译了其结构并研究了其代谢。甲状旁腺激素是一种单链多肽,由 84 个氨基酸残基组成,不含半胱氨酸,分子量约为 9500 道尔顿,在甲状旁腺中由生物前体甲状旁腺激素原 (proPTH) 形成,后者在 NH2 端有 6 个额外的氨基酸。ProPTH在甲状旁腺的主要细胞(在其颗粒内质网中)合成,并在高尔基体的蛋白水解过程中转化为甲状旁腺激素。其生物活性明显低于 PTH 的活性。显然,健康人血液中不存在 proPTH,但在病理条件下(甲状旁腺腺瘤),它可以与 PTH 一起分泌到血液中。最近,人们发现了甲状旁腺激素(proPTH)的前体——前甲状旁腺激素原(preproPTH),其在NH2末端额外含有25个氨基酸残基。因此,前甲状旁腺激素原(preproPTH)含有115个氨基酸残基,proPTH含有90个氨基酸残基,PTH含有84个氨基酸残基。
牛和猪甲状旁腺激素的结构现已完全确定。人甲状旁腺激素已从甲状旁腺腺瘤中分离出来,但其结构仅得到部分解析。甲状旁腺激素的结构存在差异,但动物和人类甲状旁腺激素表现出交叉免疫反应性。由前34个氨基酸残基组成的多肽几乎保留了天然激素的生物活性。这使得我们可以假设,羧基末端剩余的近%的分子与甲状旁腺激素的主要作用无直接关系。甲状旁腺激素的1-29片段也表现出一定的生物和免疫活性。生物无活性的53-84片段也表现出免疫作用,也就是说,甲状旁腺激素的这些特性由其分子的至少两个部分表现出来。
血液循环中的甲状旁腺激素是异质性的,与甲状旁腺分泌的天然激素不同。血液中至少存在三种不同类型的甲状旁腺激素:分子量为 9,500 道尔顿的完整甲状旁腺激素;来自甲状旁腺激素分子羧基部分的无生物活性物质,分子量为 7,000-7,500 道尔顿;以及分子量约为 4,000 道尔顿的生物活性物质。
在静脉血中发现了更小的碎片,这表明它们是在周围形成的。甲状旁腺激素碎片形成的主要器官是肝脏和肾脏。在肝脏病变和慢性肾衰竭 (CRF) 中,这些器官中的甲状旁腺激素碎片增加。在这些情况下,甲状旁腺激素碎片在血液中停留的时间明显长于健康个体。肝脏主要吸收完整的甲状旁腺激素,但不会从血液中清除羧基末端或氨基末端的甲状旁腺激素碎片。肾脏在甲状旁腺激素代谢中起主导作用。它们占羧基末端免疫反应激素代谢清除率的近 60% 和甲状旁腺激素氨基末端片段的 45%。甲状旁腺激素活性氨基末端片段的主要代谢区域是骨骼。
检测到甲状旁腺激素的脉动性分泌,夜间最强烈。夜间睡眠开始后3-4小时,其血液含量比白天平均水平高出2.5-3倍。
甲状旁腺激素的主要功能是维持钙稳态。同时,血清钙(总钙和尤其是离子钙)是甲状旁腺激素分泌的主要调节剂(钙水平降低会刺激甲状旁腺激素分泌,而钙水平升高则会抑制甲状旁腺激素分泌),即根据反馈原理进行调节。低钙血症时,甲状旁腺激素原(proPTH)转化为甲状旁腺激素的量增加。血液中的镁含量在甲状旁腺激素的释放中也起着重要作用(镁水平升高会刺激甲状旁腺激素分泌,而镁水平降低则会抑制甲状旁腺激素分泌)。甲状旁腺激素的主要作用靶点是肾脏和骨骼,但甲状旁腺激素对肠道钙吸收、碳水化合物耐受性、血脂水平的影响,以及其在阳痿、皮肤瘙痒等疾病发展中的作用已为人所知。
为了描述甲状旁腺激素对骨骼的影响,有必要提供有关骨组织结构、生理吸收和重塑特征的简要信息。
已知体内大部分钙(高达99%)存在于骨组织中。由于钙以磷钙化合物的形式存在于骨骼中,因此总磷含量的1%也存在于骨骼中。尽管骨骼组织看似静态,但其不断重塑,血管活跃,并具有较高的机械性能。骨骼是磷、镁和其他维持矿物质代谢稳态所必需的化合物的动态“仓库”。其结构包含致密的矿物质成分,这些成分与有机基质紧密相关,有机基质由90-95%的胶原蛋白、少量粘多糖和非胶原蛋白组成。骨骼的矿物质部分由羟基磷灰石(其经验式为Ca10·(PO4)·6·(OH)·2)和无定形磷酸钙组成。
骨骼由源自未分化间充质细胞的成骨细胞形成。这些单核细胞参与有机骨基质成分的合成。它们位于骨表面的单层,与类骨质紧密接触。成骨细胞负责类骨质的沉积及其随后的矿化。其生命活动的产物是碱性磷酸酶,其在血液中的含量是其活性的间接指标。在矿化的类骨质的包围下,一些成骨细胞转变为骨细胞——单核细胞,其细胞质形成与邻近骨细胞的管道相连的管道。它们不参与骨重塑,但参与骨周围骨质的破坏过程,这对于快速调节血清钙水平至关重要。骨吸收由破骨细胞——一种巨型多核细胞——进行,似乎是由单核巨噬细胞融合而成。也有人认为破骨细胞的前体可能是骨髓的造血干细胞。它们具有移动性,在骨吸收最严重的区域形成一层与骨接触的膜。破骨细胞通过释放蛋白水解酶和酸性磷酸酶,导致胶原蛋白降解、羟基磷灰石破坏以及基质中矿物质的去除。新形成的矿化程度低的骨组织(类骨质)对破骨细胞的吸收具有抵抗力。成骨细胞和破骨细胞的功能相互独立,但又相互协调,从而实现正常的骨骼重塑。骨骼长度的生长取决于软骨内骨化,而宽度和厚度的生长则取决于骨膜骨化。47Ca 的临床研究表明,骨骼中钙的总含量每年更新高达 18%。当骨骼受损(骨折、感染过程)时,改变的骨骼会被吸收并形成新骨。
参与局部骨吸收和形成过程的细胞复合物被称为基本多细胞重塑单位(BMU)。它们调节局部钙、磷和其他离子的浓度,骨有机成分(特别是胶原蛋白)的合成,以及骨的组织化和矿化。
甲状旁腺激素在骨骼中的主要作用是增强骨吸收过程,从而影响骨结构的矿物质和有机成分。甲状旁腺激素促进破骨细胞的生长及其活性,同时增强溶骨作用并增加骨吸收。在这种情况下,羟基磷灰石晶体溶解,钙和磷释放到血液中。该过程是增加血液中钙含量的主要机制。它由三个部分组成:从周围骨(深层骨细胞)动员钙;骨原细胞增殖为破骨细胞;通过调节骨骼(表层骨细胞)的钙释放来维持血液中钙的恒定水平。
因此,甲状旁腺激素最初会增加骨细胞和破骨细胞的活性,增强骨溶解作用,导致血钙水平升高,尿液中钙和羟脯氨酸的排泄增加。这是甲状旁腺激素的第一个定性、快速作用。甲状旁腺激素对骨骼的第二个作用是定量的。它与破骨细胞池的增加有关。在活跃的骨溶解作用下,会刺激成骨细胞增殖,激活以骨吸收为主的骨吸收和骨形成。甲状旁腺激素过量会导致骨平衡失衡。这伴随着羟脯氨酸的过量排泄——羟脯氨酸是胶原蛋白降解和唾液酸的产物,唾液酸包含在粘多糖的结构中。甲状旁腺激素可激活环磷酸腺苷 (cAMP)。服用甲状旁腺激素后尿液中 cAMP 排泄增加可作为组织对其敏感性的指标。
甲状旁腺激素对肾脏最重要的作用是其能够减少磷的重吸收,从而增加磷酸尿。在肾单位的不同部位,其减少机制有所不同:在近端,甲状旁腺激素的这种作用是由于通透性增加所致,并且是在cAMP的参与下发生的,而在远端,它不依赖于cAMP。甲状旁腺激素的磷酸尿作用会随着维生素D缺乏、代谢性酸中毒和磷含量降低而改变。甲状旁腺激素略微增加肾小管对钙的总重吸收。同时,它使近端钙重吸收减少,而使远端钙重吸收增加。后者起主导作用——甲状旁腺激素降低钙的清除率。甲状旁腺激素降低肾小管对钠及其碳酸氢盐的重吸收,这可能解释了甲状旁腺功能亢进时酸中毒的发生。它能促进肾脏中1,25-二氧胆钙化醇1,25(OH 2 )D 3的形成,这是维生素D 3的活性形式。这种化合物通过刺激小肠壁中一种特殊的钙结合蛋白 (CaBP) 的活性,增加小肠对钙的重吸收。
甲状旁腺激素的正常水平平均为0.15-0.6 ng/ml。该水平随年龄和性别而变化。20-29岁人群血液中甲状旁腺激素的平均含量为(0.245±0.017)ng/ml,80-89岁人群为(0.545±0.048)ng/ml;70岁女性的甲状旁腺激素水平为(0.728±0.051)ng/ml,同龄男性为(0.466±0.40)ng/ml。因此,甲状旁腺激素的含量随年龄增长而增加,但女性的增加幅度更大。
通常,应使用几种不同的测试来鉴别诊断高钙血症。
我们根据 OV Nikolaev 和 VN Tarkaeva (1974) 的分类提出了我们开发的临床和发病机制分类。
甲状旁腺激素分泌障碍及敏感性相关疾病的临床和发病学分类
原发性甲状旁腺功能亢进症
- 按发病机制分:
- 功能亢进腺瘤;
- OGD 增生;
- 功能亢进性甲状旁腺癌;
- 伴有甲状旁腺功能亢进症(Wermer 综合征)的多发性内分泌肿瘤 I 型;
- 伴有甲状旁腺功能亢进症(Sipple 综合征)的多发性内分泌肿瘤 II 型。
- 根据临床特点:
- 骨骼形态:
- 骨质疏松症,
- 纤维囊性骨炎,
- “Pagetoid”;
- 内脏病形式:
- 主要损害肾脏、胃肠道、神经精神领域;
- 混合形式。
- 骨骼形态:
- 下游:
- 辛辣的;
- 慢性的。
继发性甲状旁腺功能亢进症(甲状旁腺继发性功能亢进和增生,伴有长期低钙血症和高磷血症)
- 肾脏病理学:
- 慢性肾衰竭;
- 小管病(Albright-Fanconi型);
- 肾性佝偻病。
- 肠道病理学:
- 吸收不良综合征。
- 骨病理学:
- 老年性骨软化症;
- 产褥期;
- 特发性;
- 佩吉特病。
- 维生素D缺乏症:
- 肾脏疾病;
- 肝;
- 遗传性酶缺乏症。
- 恶性疾病:骨髓瘤。
三发性甲状旁腺功能亢进症
- 甲状旁腺的自主功能腺瘤,在长期继发性甲状旁腺功能亢进的背景下发展而来。
假性甲状旁腺功能亢进
- 非甲状旁腺来源的肿瘤产生甲状旁腺激素。
甲状旁腺激素不活跃的囊性腺和肿瘤形成
- 囊肿。
- 激素不活跃的肿瘤或癌。
甲状旁腺功能减退症
- 甲状旁腺先天性发育不全或缺失。
- 特发性、自身免疫性起源。
- 术后,与甲状旁腺切除有关。
- 术后因血液供应和神经支配受损。
- 辐射损伤,外源性和内源性(外照射放射治疗、用放射性碘治疗甲状腺疾病)。
- 因出血或梗塞导致甲状旁腺受损。
- 感染性病变。
假性甲状旁腺功能减退症
- I型——靶器官对甲状旁腺激素不敏感,依赖于腺苷酸环化酶;
- II 型 - 靶器官对甲状旁腺激素不敏感,与腺苷酸环化酶无关,可能由自身免疫引起。
假性甲状旁腺功能减退症
假性甲状旁腺功能减退症患者的家族中,健康亲属出现假性甲状旁腺功能减退症的躯体症状,且无特征性生化疾病和手足搐搦症。
 [ 13 ]、[ 14 ]、[ 15 ]、[ 16 ]、[ 17 ]、[ 18 ]、[ 19 ]、[ 20 ]、[ 21 ]
[ 13 ]、[ 14 ]、[ 15 ]、[ 16 ]、[ 17 ]、[ 18 ]、[ 19 ]、[ 20 ]、[ 21 ]
Использованная литература


