治疗严重败血症和脓毒性休克
該文的醫學專家
最近審查:04.07.2025
只有对感染部位进行全面的外科消毒并给予充分的抗菌治疗,才能有效治疗脓毒症。初始抗菌治疗不足是脓毒症患者死亡的危险因素。只有通过有针对性的重症监护,才能维持患者生命,预防和消除器官功能障碍。
其主要目标是在严重脓毒症和脓毒症休克患者氧消耗增加的情况下优化氧运输,通过血流动力学和呼吸支持进行治疗。
血流动力学支持
输液治疗
输液治疗是维持血流动力学,尤其是心输出量的初始措施之一。其在脓毒症患者中的主要任务是:
- 恢复足够的组织灌注,
- 纠正体内平衡失调,
- 细胞代谢正常化,
- 降低脓毒症级联介质和有毒代谢物的浓度。
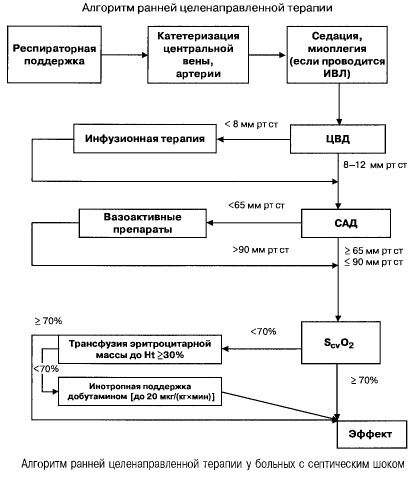
在脓毒症伴有多器官衰竭和感染性休克时,他们试图迅速(在最初6小时内)达到以下重要指标的值:
- 血细胞比容>30%,
- 利尿0.5 ml/(kgh),
- 上腔静脉或右心房血饱和度>70%,
- 平均血压>65毫米汞柱,
- 中心静脉压 8-12 毫米汞柱
将这些值维持在指定水平可提高患者生存率(B类证据)。使用Swan-Ganz导管和PICCO技术(经肺热稀释和脉搏波分析)进行血流动力学监测扩大了监测和评估血流动力学治疗效果的可能性,但尚无证据表明这些技术能够提高生存率。
最佳前负荷值需个体化选择,因为需要考虑肺内皮损伤程度、淋巴回流状态、心室舒张功能以及胸内压变化。输注治疗量的选择应确保PCWP不超过血浆COP(预防OL),且CO升高。此外,还需考虑表征肺气体交换功能的参数(paO 2和 paO 2 /FiO 2)以及X线图像的变化。
作为脓毒症和感染性休克靶向治疗的一部分,输液治疗使用晶体溶液和胶体溶液,其效果几乎相同。
所有输注介质都有其优缺点。鉴于目前实验和临床研究的结果,我们没有理由偏爱任何特定类型。
- 例如,为了充分纠正静脉回流和前负荷水平,需要输注比胶体多2-4倍的晶体液,这与体内溶液分布的特殊性有关。此外,晶体液输注与组织水肿的风险更大有关,并且其血流动力学作用比胶体短。同时,晶体液价格便宜,不影响凝血电位,不引起过敏样反应。基于上述情况,输注方案的定性组成取决于患者的特征,同时考虑到低血容量的程度、DIC综合征的阶段、外周水肿的存在和血清中白蛋白的浓度、急性肺损伤的严重程度。
- 严重BCC缺乏症患者可使用血浆替代品(葡聚糖、明胶制剂、羟乙基淀粉)。取代度为200/0.5、130/0.4和130/0.42的羟乙基淀粉比葡聚糖具有潜在优势,因为其膜逃逸风险较低,且对止血无显著的临床影响。
- 在危重情况下输入白蛋白可能会增加死亡风险。输注白蛋白期间COP的升高是暂时的,随后,在毛细血管床通透性增加的情况下(“毛细血管渗漏”综合征),白蛋白会进一步外渗。只有当血清中白蛋白浓度低于20克/升且没有“渗漏”至间质的迹象时,输注白蛋白才有可能有效。
- 冷冻血浆的使用适用于消耗性凝血病和血液凝固潜能降低。
- 由于存在发生各种并发症(急性早幼粒细胞白血病 (APL)、过敏反应等)的高风险,应限制捐献红细胞群的广泛使用。大多数专家认为,严重脓毒症患者的最低血红蛋白浓度为90-100 g/l。
纠正低血压
低灌注压需要立即启动增加血管张力和/或增强心脏收缩功能的药物。多巴胺或去甲肾上腺素是纠正脓毒症休克患者低血压的一线药物。
多巴胺(dopmin)剂量小于10 mcg/(kg·min)时,主要通过增加CO来升高血压,对全身血管阻力的影响甚微。高剂量时,其α-肾上腺素能作用占主导地位,导致动脉血管收缩;剂量小于5 mcg/(kg·min)时,多巴胺可刺激肾脏、肠系膜血管和冠状动脉的多巴胺受体,导致血管扩张、肾小球滤过率增加和Na+排泄增加。
去甲肾上腺素能升高平均动脉压,增加肾小球滤过率。其作用下,全身血流动力学得到优化,无需使用低剂量多巴胺即可改善肾功能。近年来的研究表明,与联合使用高剂量多巴胺相比,单独使用去甲肾上腺素可显著降低死亡率。
肾上腺素是一种肾上腺素能药物,其血流动力学副作用最为显著。它对心率、平均动脉压、心输出量、左心室功能以及氧气输送和消耗具有剂量依赖性的影响。然而,肾上腺素会同时引发心动过速、器官血流恶化和高乳酸血症。因此,肾上腺素的使用仅限于对其他儿茶酚胺完全无效的病例。
多巴酚丁胺是用于在正常或升高的前负荷下增加一氧化碳和氧气输送和消耗的首选药物。由于其主要作用于β1-肾上腺素受体,因此在增加这些参数方面比多巴胺更有效。
实验研究表明,儿茶酚胺除了支持血液循环外,还能通过影响关键介质的合成并产生远距离效应来调节全身炎症的进程。在肾上腺素、多巴胺、去甲肾上腺素和多巴酚丁胺的影响下,活化的巨噬细胞会减少TNF-a的合成和分泌。
肾上腺素能药物的选择按照以下算法进行:
- 心脏指数 3.5-4 l/(min x m 2 ),SvO 2 >70% - 多巴胺或去甲肾上腺素,
- 心脏指数 <3.5 l/(min x m 2 )、SvO 2 <70% - 多巴酚丁胺(如果收缩压 <70 mm Hg - 与去甲肾上腺素或多巴胺一起)。
 [ 1 ]、[ 2 ]、[ 3 ]、[ 4 ]、[ 5 ]、[ 6 ]、[ 7 ]、[ 8 ]
[ 1 ]、[ 2 ]、[ 3 ]、[ 4 ]、[ 5 ]、[ 6 ]、[ 7 ]、[ 8 ]
呼吸支持
肺是脓毒症病理过程中首批受累的靶器官之一。急性呼吸衰竭是多器官功能障碍的主要表现之一。脓毒症患者的临床和实验室表现与急性肺损伤 (ALI) 相似,随着病理过程的进展,可发展为急性呼吸窘迫综合征 (ARDS)。严重脓毒症患者是否需要机械通气取决于实质性呼吸衰竭(ARF 或 ARDS)的严重程度。其诊断标准为呼吸指数:
- <200 - 需要气管插管和呼吸支持,
- >200-读数单独确定。
如果患者在吸氧支持下自主呼吸时意识清醒,呼吸功消耗不大,心动过速不明显(心率<120次/分钟),静脉回流氧饱和度(SO2)> 90%,则可避免转入人工呼吸机。但必须密切监测患者病情。SO2 的最佳值约为90%。可通过各种气体输送方式(面罩、鼻导管)维持无毒浓度(FiO2 < 0.6)。脓毒症患者禁用无创人工呼吸机(证据类别 B)。
应避免使用高容量机械通气(MVV)模式(VO = 12 ml/kg),因为在这种情况下,肺部细胞因子的分泌会增加,从而导致多器官衰竭(MOF)加重。必须坚持安全机械通气的理念,如果满足以下条件(证据类别A),则可以实现这一点:
- 溶解氧<10毫升/公斤,
- 吸气和呼气的比例不倒置,
- 气道峰值压力<35 cm H2O,
- 氧浓度<0.6。
呼吸周期参数的选择一直进行到达到足够的机械通气为止,其标准是paO2 > 60 mm Hg,SpO2 > 88-93%,pvO2 35-45 mm Hg,SvO2 > 55%。
优化气体交换的有效方法之一是俯卧位人工通气(俯卧位)(B类证据)。该体位对于病情最危重的患者有效,但其对降低远期死亡率的效果在统计学上不显著。
营养支持
进行人工营养支持是治疗的重要组成部分,也是强制性措施之一,因为脓毒症多器官衰竭综合征的发展通常伴有代谢亢进的表现。在这种情况下,能量需求是通过破坏自身细胞结构(自噬)来满足的,这会加重器官功能障碍并增加内毒症。
营养支持被认为是在分解代谢显著增加的背景下预防严重衰竭(蛋白质-能量缺乏)的一种方法。在强化治疗方案中加入肠内营养,可以抑制肠道菌群的迁移和菌群失调,增强肠道细胞的功能活性和肠黏膜的保护作用。这些因素可以降低内毒素中毒的程度和继发感染并发症的风险。
营养支持的计算:
- 能量值-25-35千卡/(公斤体重x天),
- 蛋白质含量 - 1.3-2.0克/(公斤体重x天),
- 碳水化合物(葡萄糖)含量——低于6克/公斤/天,
- 脂肪含量-0.5-1克/公斤/天,
- 谷氨酰胺二肽0.3-0.4克/千克/天,
- 维生素 - 标准每日套装 + 维生素 K(10 毫克/天)+ 维生素 B 1和 B 6(100 毫克/天)+ 维生素 A、C、E,
- 微量元素 - 标准每日剂量+锌(15-20毫克/天+10毫克/天(如果出现稀便)),
- 电解质-Na+、K+、Ca2+根据平衡计算和血浆中的浓度。
早期开始营养支持(24-36 小时)比强化治疗的第 3-4 天更有效(B 类证据),尤其是肠内管饲。
在严重脓毒症中,肠内营养和肠外营养并无优势;器官功能障碍的持续时间、呼吸支持和正性肌力支持的持续时间相同,死亡率也相同。鉴于上述情况,早期肠内营养是比肠外营养更经济的替代方案。使用富含膳食纤维(益生元)的混合物进行管饲可显著降低严重脓毒症患者的腹泻发生率。
为了在体内有效合成蛋白质,维持代谢比率“总氮,克 - 非蛋白质热量,千卡”= 1-(110-130) 至关重要。碳水化合物的最大剂量为 6 克/(公斤体重/天),因为摄入大剂量碳水化合物可能导致高血糖症和骨骼肌分解代谢的激活。建议全天候服用脂肪乳剂。
营养支持的禁忌症:
- 失代偿性代谢性酸中毒,
- 个人对营养支持介质不耐受,
- 严重未恢复的低血容量,
- 顽固性休克 - 多巴胺剂量>15 mcg/(kg x min)且收缩压<90 mm Hg,
- 严重顽固性动脉低氧血症。
血糖控制
严重脓毒症综合治疗的一个重要方面是持续监测血浆葡萄糖浓度并进行胰岛素治疗。高血糖及其纠正需求是脓毒症患者预后不良的因素。鉴于上述情况,应维持患者血糖水平正常(4.5-6.1 mmol/l),当血糖浓度超过可接受值时,应进行胰岛素输注(0.5-1 U/h)。根据临床情况,每1-4小时监测一次血糖浓度。实施该方案后,患者生存率显著提高,且具有统计学意义。
 [ 9 ]、[ 10 ]、[ 11 ]、[ 12 ]、[ 13 ]
[ 9 ]、[ 10 ]、[ 11 ]、[ 12 ]、[ 13 ]
糖皮质激素
关于脓毒症休克患者使用糖皮质激素的有效性的现代研究结果总结如下:
- 不宜使用大剂量激素[甲基强的松龙 30-120 mg/(kg x day) 一次或连续 9 天,地塞米松 2 mg/(kg x day) 连续 2 天,倍他米松 1 mg/(kg x day) 连续 3 天] - 增加医院感染风险,对生存没有影响,
- 每天使用 240-300 毫克氢化可的松 5-7 天,可以加速血流动力学参数的稳定,允许撤回血管支持,并提高伴随相对肾上腺功能不全(证据 B 类)患者的生存率。
必须摒弃混乱的经验性泼尼松龙和地塞米松处方——没有理由将新的信息外推到这些药物上。在没有相对肾上腺功能不全的实验室证据的情况下,每日给予300毫克氢化可的松(分3-6次注射)。
- 在顽固性休克中,
- 如果需要高剂量的血管加压药来维持有效的血流动力学。
在脓毒症休克的全身炎症状态下,氢化可的松的有效性可能与激活核因子kB抑制剂(NF-kB-a)和纠正相对肾上腺功能不全有关。反过来,抑制核转录因子(NF-kB)的活性会导致诱导型NO合成酶(NO是最强的内源性血管扩张剂)、促炎细胞因子、COX和粘附分子的形成减少。
活化蛋白C
脓毒症的特征性表现之一是全身凝血功能紊乱(凝血级联激活和纤溶抑制),最终导致低灌注和器官功能障碍。活化蛋白C对炎症系统的作用通过以下几种方式实现:
- 减少选择素与白细胞的附着,从而保护内皮免受损伤,这在全身炎症的发展中起着关键作用,
- 单核细胞释放细胞因子减少,
- 阻止白细胞释放TNF-a,
- 抑制凝血酶的产生(增强炎症反应)。
抗凝、促纤溶和抗炎作用
- 激活蛋白C是由于
- Va 因子和 VIIIa 因子的降解——抑制血栓形成,
- 抑制纤溶酶原激活剂抑制剂 - 激活纤维蛋白溶解,
- 对内皮细胞和中性粒细胞有直接的抗炎作用,
- 保护内皮细胞免于凋亡
以24微克/(kg·h)的剂量连续96小时给予活化蛋白C [drotrecogin alfa (activated)] 可降低19.4%的死亡风险。给药指征:脓毒症伴急性多器官衰竭 (MOF) 且死亡风险较高(APACHE II > 25分,2个或以上器官功能障碍,B类证据)。
活化蛋白C不能降低儿童、单器官功能障碍患者、APACHE II<25分患者、非手术脓毒症患者的死亡率。
 [ 14 ], [ 15 ], [ 16 ], [ 17 ]
[ 14 ], [ 15 ], [ 16 ], [ 17 ]
免疫球蛋白
静脉注射免疫球蛋白(IgG 和 IgG+IgM)的合理性与其抑制促炎细胞因子过度作用、促进内毒素和葡萄球菌超抗原清除、消除无力状态以及增强β-内酰胺类抗生素疗效的能力相关。在严重脓毒症和脓毒症休克的治疗中,使用免疫球蛋白是唯一能够提高生存率的免疫矫正方法。IgG 和 IgM 联合使用时疗效最佳 [RR=0.48 (0.35-0.75),A 类证据]。标准给药方案为 3-5 ml/(kg x day),连续 3 天。在休克早期(“热休克”)和严重脓毒症患者(APACHE II 评分 20-25 分)中使用免疫球蛋白可获得最佳效果。
预防深静脉血栓形成
预防下肢深静脉血栓 (DVT) 对脓毒症患者的治疗结局有显著影响(A 类证据)。普通肝素和低分子肝素均可用于预防下肢深静脉血栓。低分子量肝素的主要优势在于出血并发症发生率较低、对血小板功能的影响较小以及疗效持久(可每日一次给药)。
预防胃肠道应激性溃疡的形成
这一方向对于严重脓毒症和感染性休克患者的治疗结果至关重要,因为胃肠道应激性溃疡出血的死亡率高达64-87%。如果不采取预防措施,52.8%的重症患者会发生应激性溃疡。然而,使用质子泵抑制剂和组胺H2受体阻滞剂可将风险降低两倍以上(前者比后者更有效)。预防和治疗的主要方向是将pH值维持在3.5-6.0之间。需要强调的是,除了上述药物外,肠内营养在预防应激性溃疡形成方面也发挥着重要作用。
体外血液净化
参与全身炎症发展的各种生物活性物质和代谢产物都是解毒方法的目标,这在多器官衰竭的情况下,肝肾自然清除功能缺失的情况下尤为重要。肾脏替代疗法被认为前景光明,因为它不仅可以治疗肾衰竭患者的尿毒症,还可以对脓毒症、休克和多器官衰竭中出现的其他体内平衡变化和器官功能障碍产生积极影响。
迄今为止,尚无数据证实体外血液净化技术作为脓毒症和脓毒症休克病因治疗的主要方向之一的必要性。在以肾脏为主的多器官衰竭病例中,使用体外血液净化技术是合理的。
 [ 18 ]、[ 19 ]、[ 20 ]、[ 21 ]、[ 22 ]、[ 23 ]
[ 18 ]、[ 19 ]、[ 20 ]、[ 21 ]、[ 22 ]、[ 23 ]
血液透析
该方法的本质是低分子量物质(分子量最高可达5x10 3 Da)通过半透膜扩散,并沿着压力梯度将体内多余的液体排出。血液透析广泛用于治疗慢性和急性肾衰竭患者。物质的扩散速率与其分子量呈指数关系。例如,寡肽的去除速度比其合成速度慢。
血液滤过
血液滤过是去除分子量为5x10 3 - 5x10 4 Da的物质的有效方法,也是从体内清除大量生物活性物质和代谢物的唯一方法。该方法基于对流传质原理。除了充分纠正氮质血症外,血液滤过还能有效清除过敏毒素C3a、C5a、促炎细胞因子(TNF-a、IL-1b、6和8)、β2-微球蛋白、肌红蛋白、甲状旁腺激素、溶菌酶(分子量-6000 Da)、α-淀粉酶(分子量-36,000-51,000 Da)、肌酸磷酸激酶、碱性磷酸酶、转氨酶等物质。血液滤过还能清除氨基酸和血浆蛋白(包括免疫球蛋白和循环免疫复合物)。
血液透析滤过
血液透析滤过是最有效的血液净化方法,它结合了扩散和对流(即GD和GF)。病理物质在滤膜上的吸附也有助于解毒过程。
血浆置换
血浆置换(血浆交换,血浆滤过)也被认为是纠正脓毒症和脓毒症休克患者全身炎症的一种可能方法。最佳方法是连续进行血浆置换,取出3-5倍体积的血浆,同时用新鲜冰冻血浆、白蛋白、胶体和晶体溶液替换。血浆滤过的筛分系数为1,可有效去除C反应蛋白、结合珠蛋白、补体片段C3、α-抗胰蛋白酶、白介素-6、血栓素-B2、粒细胞刺激因子和肿瘤坏死因子(TNF)。使用吸附剂净化患者血浆可降低感染风险,并降低操作成本,因为无需使用外来蛋白。
在严重脓毒症中,使用 1000 mcg/天的长期输注亚硒酸钠(硒酶)可降低死亡率。
硒是人体必需的微量元素,其重要性与其在细胞抗氧化系统中的关键作用相关。血液中的硒含量维持在1.9-3.17 μM/l之间。人体每日硒需求量为50-200 μg,这取决于其他抗氧化剂和微量元素的供应情况。
硒是一种强抗氧化剂,是谷胱甘肽过氧化物酶、磷酸化谷胱甘肽过氧化物酶、其他氧化还原酶和一些转移酶的组成部分,其中谷胱甘肽过氧化物酶是内源性抗氧化系统中最重要的环节。
近年来,人们对硒在危急情况下的有效性进行了研究。这些研究表明,硒的主要作用机制是:
- 抑制 NF-kB 过度活化;
- 补体活化降低;
- 其作为免疫调节剂、抗氧化剂和抗炎剂的作用
- 维持过氧化物的利用率;
- 抑制内皮细胞粘附(降低 ICAM-1、VCAM-2 的表达,
- E - 选择素,P - 选择素);
- 保护内皮免受氧自由基的侵害(使用硒蛋白 P,可防止 O2和NO形成过氧亚硝酸盐)。
综上所述,我们可以明确严重脓毒症重症监护的具体任务:
- 血流动力学支持:中心静脉压8~12mmHg,平均血压>65mmHg,利尿0.5ml/(kg·h),红细胞压积>30%,混合静脉血饱和度>70%。
- 呼吸支持峰值气道压力<35 cm H2O,吸气氧分数<60%,潮气量<10 ml/kg,非倒置吸气呼气比率。
- 糖皮质激素 - “低剂量”(氢化可的松每天 240-300 毫克)。
- 严重脓毒症 (APACHE II >25) 患者活化蛋白 C 24 mcg/(kg h) 持续 4 天。
- 使用五珠蛋白进行免疫矫正替代疗法。
- 预防下肢深静脉血栓形成。
- 预防胃肠道应激性溃疡的形成:使用质子泵抑制剂和H2-组胺受体阻滞剂。
- 急性肾衰竭的替代疗法。
- 营养支持:食物能量值25-30 kcal/kg体重x天),蛋白质1.3-2.0 g/(kg体重x天),谷氨酰胺二肽0.3-0.4 g/(kgx天),葡萄糖-非蛋白质热量的30-70%,前提是血糖维持在<6.1 mmol/l,脂肪-非蛋白质热量的15-50%。


