囊性纤维化
該文的醫學專家
最近審查:04.07.2025
囊性纤维化是一种常染色体隐性单基因遗传病,以重要器官外分泌腺分泌功能障碍为特征,主要损害呼吸系统和消化系统,病程严重,预后不良。
 [ 1 ]
[ 1 ]
發病
囊性纤维化基因突变会破坏一种名为CFTR(囊性纤维化跨膜调节蛋白)的蛋白质的结构和功能。这种蛋白质作为氯离子通道,参与支气管肺系统、胃肠道、胰腺、肝脏和生殖系统上皮细胞的水-电解质交换。由于CFTR蛋白的功能和结构被破坏,氯离子(Cl-)会在细胞内积聚。这会导致排泄管腔内电位发生变化,促使大量钠离子(Na +)从管腔流入细胞,并进一步增强细胞周围空间对水的吸收。
由于这些变化,大多数外分泌腺的分泌物变稠,其排出受到干扰,导致器官和系统出现明显的继发性疾病,最明显的是支气管肺和消化系统。
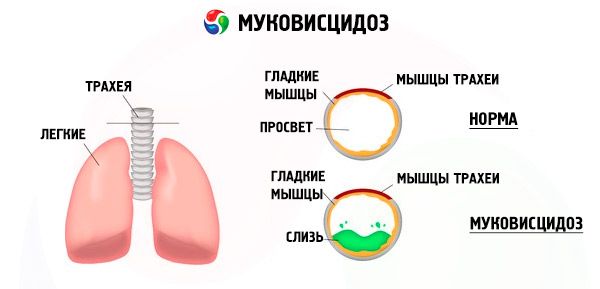
支气管内出现不同程度的慢性炎症,纤毛上皮功能严重受损,痰液变得非常粘稠、浓稠,难以排出,出现痰液淤积,并形成支气管扩张和支气管扩张,且随着时间的推移,支气管扩张会逐渐增多。这些变化导致缺氧加重,并最终导致慢性肺源性心脏病的发生。
囊性纤维化患者极易发生支气管肺部系统慢性炎症。这是由于局部支气管肺部防御系统明显紊乱(IgA、干扰素水平降低,以及肺泡巨噬细胞和白细胞的吞噬功能下降)。
肺泡巨噬细胞在支气管肺部系统慢性炎症的形成中起着重要作用。它们产生大量的IL-8,这显著增强了支气管树中中性粒细胞的趋化作用。中性粒细胞在支气管中大量聚集,并与上皮细胞一起分泌多种促炎细胞因子,包括IL-1、IL-8、IL-6、肿瘤坏死因子和白三烯。
弹性蛋白酶的高活性在支气管肺系统损伤的发病机制中也起着重要作用。弹性蛋白酶分为外源性和内源性。前者由细菌菌群(尤其是铜绿假单胞菌)产生,后者由中性粒细胞产生。弹性蛋白酶会破坏支气管上皮和其他结构元素,进一步破坏粘膜纤毛运输,并迅速导致支气管扩张。
中性粒细胞还会分泌其他蛋白水解酶。α-1-抗吡嗪和白蛋白蛋白酶的分泌抑制剂可以抵消蛋白水解酶的影响,从而保护支气管肺系统免受其损害。然而,不幸的是,在囊性纤维化患者中,这些保护性因素被大量的中性粒细胞蛋白酶抑制。
所有这些情况都会导致感染进入支气管肺部系统,并发展为慢性化脓性支气管炎。此外,还应考虑到囊性纤维化基因编码的缺陷蛋白会改变支气管上皮的功能状态,这有利于细菌(主要是铜绿假单胞菌)粘附在支气管上皮上。
囊性纤维化除了支气管肺系统的病变外,还会对胰腺、胃、大肠、小肠和肝脏造成严重损害。
症狀 纤维囊泡症
囊性纤维化可表现为多种临床症状。新生儿可出现胎粪性肠梗阻。由于胰蛋白酶缺乏甚至完全缺失,胎粪会变得非常浓稠,并积聚在回盲部。此外,还会出现肠梗阻,表现为剧烈呕吐(伴有胆汁)、腹胀、胎粪排泄困难、出现腹膜炎症状以及严重中毒综合征的临床症状迅速加重。如果不进行紧急手术干预,患儿可能在出生后数日内死亡。
在不太严重的病例中,囊性纤维化的典型症状是排便量多、次数多、油性大便,含有大量脂肪,并伴有难闻的气味。1/3的患者可出现直肠脱垂。
随后,患者继续出现肠道功能障碍、吸收不良综合征、严重的身体发育障碍和严重的维生素缺乏症。
在出生后一到两岁,支气管肺系统损伤的症状(轻度疾病)开始出现,其表现为咳嗽,可能非常明显,类似于百日咳。咳嗽伴有紫绀、呼吸急促以及痰液粘稠(最初为粘液性,后转为脓性)。逐渐出现慢性阻塞性支气管炎和支气管扩张、肺气肿和呼吸衰竭的临床表现。儿童极易感染急性呼吸道病毒和细菌感染,这会导致支气管肺部病变加重和进展。还可能发展为感染依赖性支气管哮喘。
在学龄儿童中,囊性纤维化可能表现为“肠绞痛”。患者主诉剧烈阵发性腹痛、腹胀和反复呕吐。腹部触诊可在大肠投影处发现致密结构——粪便团块与浓稠粘液混合。由于儿童在炎热天气下汗液排出过多盐分,极易发生低氯性碱中毒,皮肤上会出现“盐霜”。
成人支气管肺系统疾病
囊性纤维化(肺部疾病)患者的支气管肺系统损害的特征是出现慢性化脓性阻塞性支气管炎、支气管扩张、慢性肺炎、肺气肿、呼吸衰竭和肺心病。部分患者可出现气胸和囊性纤维化的其他并发症,例如肺不张、肺脓肿、咯血、肺出血和感染依赖性支气管哮喘。
患者主诉阵发性疼痛性咳嗽,咳出粘稠、难以分离的脓性黏痰,有时还混有血液。此外,患者极易出现气短,首先在体力活动时出现,然后是在休息时。气短是由支气管阻塞引起的。许多患者主诉息肉和鼻窦炎引起的慢性鼻炎。显著虚弱、进行性体力下降、频繁出现急性呼吸道病毒性疾病也是患者的特征。体格检查时,应注意皮肤苍白、面部浮肿、可见黏膜发绀以及严重的气短。随着失代偿性肺心病的发展,腿部会出现水肿。手指末端指骨增厚呈鼓槌状,指甲呈表面玻璃状。胸部呈桶状(由于肺气肿的发展)。
肺部叩诊可发现肺气肿的体征:箱音、肺缘活动度急剧受限以及肺下缘降低。肺部听诊可发现呼吸困难,呼气延长,散在干性哮鸣音,以及湿性、中度至细小气泡性哮鸣音。重度肺气肿患者呼吸会急剧减弱。
囊性纤维化的肺外表现
囊性纤维化的肺外表现可能非常明显并且经常发生。
胰腺损伤
85% 的囊性纤维化患者会出现不同程度的胰腺外分泌功能障碍。胰腺损伤轻微时,不会出现消化不良和吸收不良综合征,仅会出现外分泌功能障碍的实验室检查结果(血液和十二指肠内容物中胰蛋白酶和脂肪酶含量低;常伴有严重的脂肪泻)。已知仅分泌 1% 至 2% 的总脂肪酶即可预防消化不良综合征。只有严重的外分泌功能障碍才会出现临床表现。
正常情况下,胰腺腺泡会产生富含酶的液体分泌物。分泌物在排泄管中流动时,会富含水分和阴离子,使其变得更加稀薄。囊性纤维化时,由于跨膜调节器(氯离子通道)的结构和功能发生紊乱,胰腺分泌物得不到足够的液体,变得粘稠,其在排泄管中的流动速度急剧减慢。分泌物的蛋白质沉积在小排泄管壁上,导致其阻塞。随着病情进展,最终导致腺泡破坏和萎缩,形成伴有胰腺外分泌功能不全的慢性胰腺炎。临床表现为消化不良和吸收不良综合征。胰腺功能不全是囊性纤维化患者脂肪吸收不良的主要原因,但这通常伴有严重的脂肪酶缺乏。Forsher 和 Durie(1991)指出,在完全缺乏胰腺脂肪酶的情况下,脂肪分解吸收率仅为 50% 至 60%,这是由于胃和唾液(舌下)脂肪酶的存在,其活性接近正常值的下限。除了脂肪分解和吸收受阻外,蛋白质分解和重吸收也会受阻。约 50% 的食物蛋白质会随粪便排出。尽管缺乏 α-淀粉酶,碳水化合物吸收受到的影响较小,但碳水化合物代谢可能会受到严重干扰。
胰腺损害表现为消化不良和吸收不良综合征,伴有体重明显下降和大量脂肪便。
肠道腺体严重功能障碍、肠液分泌受损以及肠道酶含量减少也会促进消化不良和吸收不良综合征的发展。
消化不良和吸收不良综合征也称为肠道囊性纤维化。
晚期囊性纤维化患者(2% 的儿童和 15% 的成人)会出现胰腺内分泌功能受损(糖尿病)
 [ 16 ], [ 17 ], [ 18 ], [ 19 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ]
肝脏和胆道损伤
13% 的混合型和肠型囊性纤维化患者会发展为肝硬化。W128X、delta-P508 和 X1303K 突变是最常见的肝硬化特征。5%-10% 的患者可诊断为胆汁性肝硬化伴门静脉高压。根据 Welch, Smith (1995) 的研究,86% 的囊性纤维化患者可检测到肝损伤的临床、形态学、实验室和仪器检查体征。
许多囊性纤维化患者还会患上慢性胆囊炎,通常是结石性胆囊炎。
性腺功能障碍
囊性纤维化患者可能会出现无精子症,这是导致不孕不育的原因。女性生育能力下降也是很常见的情况。
階段
肺囊性纤维化的严重程度分为三个等级。
轻度囊性纤维化的特点是很少发作(每年不超过一次);在缓解期间,临床表现几乎不存在,患者能够工作。
中度严重程度——每年发作2-3次,每次持续约2个月或更长时间。发作期症状包括剧烈咳嗽,痰液难以咳出,轻微体力活动后呼吸困难,体温偏低,全身乏力,出汗。同时,胰腺外分泌功能受损。缓解期,胰腺功能尚未完全恢复,体力活动后呼吸困难仍然存在。
重症病程的特点是病情反复发作,几乎无法缓解。临床表现为严重呼吸衰竭、慢性肺源性心脏病症状(常失代偿),咯血是典型症状。患者体重明显下降,甚至完全丧失行动能力。严重的支气管肺部病变通常伴有明显的胰腺功能障碍。
形式
- 支气管肺部病变
- 反复发作的肺炎,病程迁延。
- 脓肿性肺炎,尤其是婴儿。
- 慢性肺炎,尤其是双侧肺炎。
- 对传统疗法无效的支气管哮喘。
- 复发性支气管炎、细支气管炎,尤其是有铜绿假单胞菌培养。
- 胃肠道变化
- 胎粪性肠梗阻及其等同症状。
- 原因不明的肠道吸收功能受损综合征。
- 新生儿阻塞性黄疸,病程迁延。
- 肝硬化。
- 糖尿病。
- 胃食管反流。
- 胆结石。
- 直肠脱垂。
- 其他器官和系统的变化
- 生长和发育障碍。
- 性发育迟缓。
- 男性不育。
- 鼻息肉。
- 来自囊性纤维化家族的兄弟姐妹。
 [ 24 ]
[ 24 ]
診斷 纤维囊泡症
一般血液分析:常见不同程度贫血,通常为正常或低色素性贫血。贫血的成因多种多样(由于吸收不良综合征导致肠道对铁和维生素B12的吸收减少)。化脓性支气管炎和肺炎可能导致白细胞减少,白细胞增多,血沉增快。
一般尿液分析 - 无明显变化,在极少数情况下观察到轻微蛋白尿。
粪便检查 - 可观察到脂肪泻和腹泻。Becker(1987)建议测量粪便中的糜蛋白酶和脂肪酸。在测量粪便中的糜蛋白酶之前,必须在检查前至少3天停止服用消化酶。囊性纤维化患者粪便中的糜蛋白酶含量减少,脂肪酸含量增加(正常的脂肪酸排泄量低于20 mmol/天)。需要注意的是,以下情况也会出现粪便中脂肪酸排泄量的增加:
- 由于肝功能衰竭、胆管阻塞、小肠细菌大量定植(在这种情况下,胆汁酸会发生剧烈水解)导致小肠共轭脂肪酸缺乏;
- 回肠炎;
- 乳糜泻(伴有吸收不良综合征的发展);
- 肠炎;
- 肠道淋巴瘤;
- 惠普尔病;
- 食物过敏;
- 各种原因引起的腹泻、类癌综合征、甲状腺机能亢进症中食物团块的加速运输。
生化血液测试-总蛋白和白蛋白水平降低,α2和γ球蛋白、胆红素和氨基转移酶水平升高(肝损伤的情况下),淀粉酶、脂肪酶、胰蛋白酶活性以及铁和钙水平降低(消化不良综合征、吸收不良的情况下)。
痰液分析 - 存在大量中性粒细胞和微生物(痰液细菌学检查期间)。
对小肠的吸收功能和胰腺的外分泌功能的研究发现了明显的紊乱。
肺部X光检查 - 发现变化,其严重程度取决于疾病的严重程度和阶段。最具特征性的变化是:
- 由于支气管周围间质变化导致肺部模式增加;
- 肺根扩张;
- 肺小叶、亚段或甚至段性肺不张的图片;
- 肺部透明度增加,主要在上部,膈肌位置较低且活动性不足,胸骨后空间扩张(肺气肿的表现);
- 肺组织节段性或多节段性浸润(在肺炎的发展中)。
支气管造影可显示由于粘稠痰液阻塞支气管而引起的变化(造影剂使支气管填充物碎裂、轮廓不均匀、支气管破裂现象、侧支数量明显减少)以及主要位于肺下部的支气管扩张(圆柱形、混合形)。
支气管镜检查发现弥漫性化脓性支气管炎,有大量浓稠粘稠的痰液和纤维素膜。
肺量计检查 - 在疾病的早期阶段就已经发现阻塞型(FVC、FEV1、Tiffno 指数下降)、限制型(FVC 下降)或最常见的是阻塞限制型(FVC、FVC、FEV1、Tiffno 指数下降)呼吸衰竭。
Gibson 和 Cook 汗液测试(汗液电解质测试)是利用毛果芸香碱电泳刺激出汗,然后测定汗液中的氯化物。Doerehuk(1987)对该测试进行了如下描述。毛果芸香碱电泳在前臂进行,电流为 3 mA。用蒸馏水清洁皮肤后,将滤纸放在刺激区域收集汗液,并用纱布覆盖以防止汗液蒸发。30-60 分钟后,取下滤纸,用蒸馏水洗脱。测量收集到的汗液量。为了获得可靠的结果,至少需要收集 50 毫克(最好是 100 毫克)的汗液。
如果氯化物浓度超过60 mmol/l,则诊断囊性纤维化的可能性较大;如果氯化物浓度超过100 mmol/l,则诊断可靠;在这种情况下,氯和钠浓度的差异不应超过8-10 mmol/l。Hadson(1983)建议,如果汗液中钠和氯化物含量处于临界值,应进行泼尼松龙试验(口服5毫克,持续2天,然后测定汗液中的电解质)。对于未患囊性纤维化的个体,汗液中的钠含量会降至正常下限;而囊性纤维化个体则不会发生变化。建议所有患有慢性咳嗽的儿童进行汗液试验。
通过血斑或DNA样本分析囊性纤维化基因的主要突变是最敏感和最特异的诊断检测。然而,这种方法仅适用于delta-P508突变率高于80%的国家。此外,该技术成本高昂,技术复杂。
囊性纤维化的产前诊断是通过测定羊水中碱性磷酸酶的同工酶来进行的。这种方法在妊娠18-20周时即可进行。
诊断囊性纤维化的主要标准如下:
- 有儿童期身体发育迟缓、反复发作的慢性呼吸道疾病、消化不良和腹泻、近亲属有囊性纤维化病史的迹象;
- 慢性阻塞性支气管炎,常复发,随着支气管扩张和肺气肿的发展,常发生复发性肺炎;
- 慢性复发性胰腺炎,外分泌功能明显下降,吸收不良综合征;
- 患者汗液中的氯含量增加;
- 不孕症,但性功能尚可。
通过识别风险群体,可以成功诊断和鉴别诊断囊性纤维化。
囊性纤维化筛查计划
- 血液、尿液、痰液的一般分析。
- 痰液的细菌学分析。
- 粪便学分析。
- 生化血液检查:总蛋白及蛋白组分、葡萄糖、胆红素、氨基转移酶、碱性磷酸酶、γ-谷氨酰转肽酶、钾、钙、铁、脂肪酶、淀粉酶、胰蛋白酶的测定。
- 研究胰腺的外分泌功能和肠道的吸收功能。
- 肺部透视和放射线照相术、肺部 CT 扫描。
- 心电图。
- 超声心动图。
- 支气管镜检查和支气管造影。
- 肺量测定。
- 汗液測試。
- 咨询遗传学家。
- 分析血斑或 DNA 样本以发现囊性纤维化基因的主要突变。
誰聯繫?
治療 纤维囊泡症
囊性纤维化症状的类型和严重程度可能有很大差异,因此没有典型的治疗方案;治疗方案是针对每个人的个体化治疗。
该疗法包括以下治疗措施:
- 呼吸练习和体位引流有助于清除肺部积聚的浓稠黏液。一些呼吸道清理技巧需要家人、朋友或肺科医生的帮助。许多人会使用高频振动的充气胸部背心。

- 具有支气管扩张、引流(粘液溶解)和抗菌作用的吸入药物(例如氟喹诺酮类药物)。
- 含有胰腺酶的制剂,可促进消化。这些制剂可在用餐时服用。
- 多种维生素(包括脂溶性维生素)。
2015年,FDA批准了第二种治疗囊性纤维化的药物,该药物靶向一种名为CFTR的缺陷蛋白。第一种药物,即所谓的CFTR调节剂,于2012年获得批准。CFTR调节剂有望将部分囊性纤维化患者的寿命延长数十年。
可能需要手术来治疗以下呼吸道并发症:
- 气胸、大量复发性或持续性咯血、鼻息肉、持续性和慢性鼻窦炎。
- 胎粪性肠梗阻、肠套叠、直肠脱垂。
肺移植是在疾病的终末阶段进行的。


