杭丁顿舞蹈症
該文的醫學專家
最近審查:05.07.2025
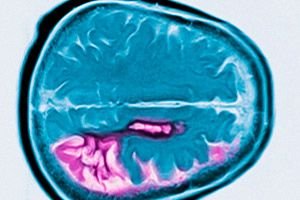
亨廷顿氏病是一种常染色体显性遗传性神经退行性疾病,其特征为中年起出现进行性认知衰退、不自主运动和运动协调障碍。诊断需通过基因检测确诊。治疗主要针对症状。血亲可能建议进行基因检测。乔治·亨廷顿于1872年在研究了长岛居民的一个家庭病例后首次描述了这种疾病。
亨廷顿舞蹈症的发病率约为每十万人10例,由于发病较晚,每十万人中约有30人一生中有50%的风险患上此病。虽然这种疾病最常发病于35至40岁之间,但发病年龄范围很广,最早发病为3岁,最晚为90岁。虽然最初认为这种疾病具有100%的外显率,但现在认为并非总是如此。从父亲遗传了致病基因的人比从母亲遗传了致病基因的人平均早3年发病。在从父亲遗传了致病基因的患者中,约有80%的人在20岁之前发病。后代较早表现出基因缺陷的现象称为预期。
 [ 1 ]
[ 1 ]
亨廷顿氏病的病因是什么?
亨廷顿舞蹈症不分性别。该病表现为尾状核萎缩,小神经元退化,神经递质——γ-氨基丁酸 (GABA) 和 P 物质——水平下降。
一个突变基因,其编码的氨基酸谷氨酰胺的CAG(半胱氨酸-丙氨酸-甘氨酸)DNA序列数量增加(“扩增”),是导致亨廷顿舞蹈症发生的元凶。该基因的产物,大型蛋白亨廷顿蛋白,含有过量的多聚谷氨酰胺残基,通过未知机制导致该疾病。CAG重复次数越多,疾病出现得越早,病程也越严重。随着代代相传,重复次数会不断增加,随着时间的推移,会导致家族表型的恶化。
尽管人们对帕金森病的遗传和生化变化非常感兴趣,但直到 20 世纪 70 年代末,寻找该疾病基因的努力才得以成功。当时,南希·韦克斯勒和艾伦·托宾组织了一场由遗传病基金会赞助的研讨会,讨论寻找亨廷顿舞蹈症基因的策略。与会的大卫·豪斯曼、大卫·博特斯坦和雷·怀特提出,当时开发的重组 DNA 技术可能有助于实现这一目标。该项目的一项关键任务是找到一个世代患有亨廷顿舞蹈症的大家族以获取 DNA 样本。1979 年,委内瑞拉和美国科学家启动了一个联合项目,对居住在马拉切博湖(委内瑞拉)岸边的一个患有亨廷顿舞蹈症的大家族进行检查。 1983年,亨廷顿氏病基因被定位于4号染色体短臂末端(Gusella等人,1983年)。十年后,人们发现该基因突变是由胞嘧啶-腺嘌呤-鸟嘌呤(CAG)三核苷酸重复次数增加引起的(亨廷顿氏病合作研究小组,1993年)。该科研小组开发的方法目前被认为是新基因定位克隆的标准。
野生型基因的 CAG 重复序列为 10-28 个,而导致亨廷顿舞蹈症的基因突变形式的 CAG 重复序列从 39 个增加到 100 个以上。三核苷酸重复序列扩增的发现有助于解释该疾病的许多临床特征。特别是,研究发现发病年龄与三核苷酸重复区域的长度呈负相关。男性在精子发生过程中重复次数的增加常常可以解释对父系遗传的预期。对新突变的分析表明,它们通常发生在父母一方(通常是父亲)的 CAG 重复次数高于 28 时;在这种情况下,这些重复次数在下一代会增加。现在已经确定,如果重复次数不超过 28,它就会稳定地代代相传。如果重复次数在29到35之间,亨廷顿舞蹈症的症状不会出现,但遗传给后代后,该区域的长度可能会增加。如果重复次数在36到39之间,则在某些情况下(但并非总是如此),疾病可能会在临床上表现出来(不完全外显率),并且遗传给后代后,三核苷酸重复次数可能会增加。如果重复次数超过40,则几乎所有病例都会发病,并且遗传给后代后,重复次数可能会进一步增加。重复次数增加的原因尚不清楚。
亨廷顿舞蹈症的病理形态学
亨廷顿舞蹈症的特征是神经元主要丢失在尾状核和壳核中,在一定程度上也丢失在皮层和其他脑结构中。亨廷顿舞蹈症患者的脑总重量不仅由于神经元数量的减少而减少,还由于白质的损失而减少。在大脑皮层中,第五层和第六层的细胞受影响最严重。微观和宏观退行性病变的严重程度(根据死亡年龄调整)与CAG重复次数相关。对数百例亨廷顿舞蹈症病例的详细病理分析表明,纹状体的退化始于尾状核的背内侧部分和壳核的背外侧部分,然后向腹侧扩散。尾状核和壳核中不同组神经元受到的影响程度不同。纹状体中的中间神经元保持相对完整,但一些投射神经元受到选择性影响。在青少年型亨廷顿舞蹈症中,纹状体的病理形态学改变更为明显且更为广泛,涉及大脑皮层、小脑、丘脑和苍白球。
亨廷顿舞蹈症的神经化学变化
GABA。对亨廷顿氏病患者脑部的神经化学研究表明,纹状体中GABA浓度显著下降。后续研究证实,亨廷顿氏病与GABA能神经元数量减少有关,并表明GABA浓度不仅在纹状体中降低,在其投射区(苍白球内外节和黑质)也降低。在亨廷顿氏病患者的脑部,通过受体结合研究和mRNA原位杂交也检测到了GABA受体的变化。尾状核和壳核中的GABA受体数量略有减少,但在黑质网状部分和苍白球外节中有所增加,这可能是由于失神经支配的过敏反应所致。
乙酰胆碱。乙酰胆碱被纹状体中大型无棘中间神经元用作神经递质。早期对亨廷顿舞蹈症患者的尸检研究表明,纹状体中胆碱乙酰转移酶 (ChAT) 活性降低,提示胆碱能神经元丢失。然而,与 GABA 能神经元的显著减少相比,胆碱能中间神经元相对较少。因此,与年龄匹配的对照组相比,纹状体中乙酰胆碱酯酶阳性神经元的密度和 ChAT 活性实际上相对升高。
P物质。P物质存在于纹状体的许多中等大小的棘状神经元中,这些神经元主要投射到苍白球内节和黑质,通常也含有强啡肽和γ-氨基丁酸(GABA)。亨廷顿氏病患者的纹状体和黑质网状部中的P物质水平会降低。免疫组织化学研究表明,在疾病的终末期,含有P物质的神经元数量显著减少。在早期阶段,与投射到黑质网状部的神经元相比,投射到苍白球内节的含有P物质的神经元相对较少。
阿片类肽。脑啡肽存在于间接通路中中等棘状投射GABA能神经元中,这些神经元投射至苍白球外节,并携带D2受体。免疫组织化学研究表明,在亨廷顿舞蹈症早期,投射至苍白球外节的含脑啡肽神经元会丢失。这些细胞的死亡时间似乎比投射至苍白球内节的含P物质的细胞更早。
儿茶酚胺。含有生物胺(多巴胺、血清素)并投射至纹状体的神经元位于黑质致密部、腹侧被盖和缝核。虽然人类纹状体的去甲肾上腺素能投射很少,但纹状体中的血清素和多巴胺水平(每克组织)升高,这表明尽管纹状体自身神经元明显丢失,但这些传入投射仍然保留。在经典型和幼年型亨廷顿舞蹈症中,黑质的多巴胺能神经元均保持完整。
生长抑素/神经肽Y和一氧化氮合成酶。对亨廷顿舞蹈症患者纹状体中生长抑素和神经肽Y水平的测量显示,与正常组织相比,纹状体中生长抑素和神经肽Y水平升高了4-5倍。免疫组织化学研究表明,含有神经肽Y、生长抑素和一氧化氮合成酶的纹状体中间神经元完全保留。因此,这些神经元对病理过程具有抵抗力。
兴奋性氨基酸。有人认为,亨廷顿氏病的选择性细胞死亡是由于谷氨酸诱导的神经毒性作用所致。亨廷顿氏病患者纹状体中的谷氨酸和喹啉酸(一种内源性神经毒素,是血清素代谢的副产物,也是谷氨酸受体的激动剂)水平略有改变,但最近一项使用磁共振波谱的研究显示,体内谷氨酸水平升高。亨廷顿氏病患者纹状体中负责合成喹啉酸的神经胶质酶水平比正常人高出约5倍,而确保喹啉酸降解的酶活性在亨廷顿氏病患者中仅高出20%至50%。因此,亨廷顿氏病患者中喹啉酸的合成可能增加。
亨廷顿舞蹈症中兴奋性氨基酸 (EAA) 受体的研究表明,纹状体中的 NMDA 受体、AMPA 受体、海人酸受体和代谢型谷氨酸受体数量显著减少,大脑皮层中的 AMPA 受体和海人酸受体数量也显著减少。在亨廷顿舞蹈症晚期,NMDA 受体几乎消失,而在临床前和早期,这些受体的数量显著减少。
选择性敏感性。在亨廷顿舞蹈症中,某些类型的纹状体细胞会选择性地丢失。中等棘状神经元,它们投射到苍白球外部节,并含有GABA和脑啡肽,在疾病早期就死亡,同样死亡的还有含有GABA和P物质并投射到黑质网状部的神经元。投射到苍白球外部节的含有GABA和脑啡肽的神经元的丢失,会解除该结构的抑制,进而导致丘脑底核的活性抑制。丘脑底核活动的减少似乎可以解释亨廷顿舞蹈症中出现的舞蹈样运动。人们早已知道丘脑底核的局部病变可导致舞蹈病。投射至黑质网状部的GABA和P物质神经元的缺失可能是亨廷顿舞蹈症患者眼球运动障碍的病因。该通路通常会抑制投射至上丘的黑质网状部神经元,而上丘神经元则负责调节扫视。在青少年亨廷顿舞蹈症中,上述通路受到的影响更为严重,此外,纹状体向苍白球内节的投射也会提前消失。
亨廷顿蛋白(huntingtin)由导致亨廷顿舞蹈症的基因突变编码,存在于大脑和其他组织的各种结构中。亨廷顿蛋白通常主要存在于神经元的细胞质中。该蛋白存在于大脑的大多数神经元中,但最近的数据显示,其在基质神经元中的含量高于纹状体神经元,在投射神经元中的含量高于中间神经元。因此,神经元的选择性敏感性与其亨廷顿蛋白含量相关,而亨廷顿蛋白通常存在于某些神经元群体中。
与亨廷顿氏病患者的大脑一样,在转基因小鼠中,如果该小鼠携带亨廷顿氏病基因N末端片段,且重复序列数量增加,亨廷顿蛋白会在神经元细胞核内形成致密的聚集物。这些核内包涵体在纹状体投射神经元中形成(但不在中间神经元中形成)。在转基因小鼠中,这些包涵体在症状出现前数周就已形成。这些数据表明,含有更多谷氨酰胺残基(其包涵体编码三核苷酸重复序列)的亨廷顿蛋白或其片段会在细胞核中积聚,并可能因此削弱其对细胞功能的控制。
亨廷顿舞蹈症的症状
由于亨廷顿舞蹈症患者发病的年龄难以准确确定,因为该病的发病过程是渐进性的。在出现更明显的症状之前,患者可能多年前就出现了性格和行为的改变以及轻微的协调障碍。确诊时,大多数患者会出现舞蹈样运动、精细运动协调性受损以及自主扫视功能减退。随着病情发展,患者组织活动的能力会受损,记忆力下降,言语障碍,眼球运动障碍和协调运动能力下降的情况会加重。虽然在疾病早期,患者不会出现肌肉和姿势的变化,但随着病情的发展,可能会出现肌张力障碍,并随着时间的推移逐渐成为主要症状。在晚期,患者会出现言语不清、吞咽困难,甚至无法行走。亨廷顿舞蹈症通常需要15-20年的时间才能痊愈。在终末期,患者将无助地生活,需要持续的护理。死亡结果与原发疾病没有直接关系,而是与其并发症有关,例如肺炎。
亨廷顿氏病引起的痴呆
ICD-10代码
P02.2. 亨廷顿氏病引起的痴呆(G10)。
痴呆症是系统性退行性萎缩的表现之一,主要损害大脑纹状体系统和其他盲肠下核。痴呆症是一种常染色体显性遗传病。
通常,这种疾病在三四十岁时表现出舞蹈样运动功能亢进(特别是在面部,手臂,肩膀,步态),人格改变(兴奋,歇斯底里和分裂型人格异常),精神病(特殊的抑郁症,伴有忧郁,阴沉,烦躁不安;偏执情绪)。
舞蹈样运动功能亢进、痴呆和遗传因素的结合对于诊断尤为重要。以下是针对此类痴呆的具体诊断:
- 进展缓慢(平均 10-15 年):剩余的自我照顾能力与在需要进行生产性脑力劳动(概念思维、学习新事物)的情况下明显的智力缺陷之间的分离;
- 精神表现明显不平衡,这是基于注意力的严重障碍和患者态度的不稳定(“急促”的思维,类似于运动功能亢进);
- 高级皮质功能明显受损的非典型性;
- 痴呆症的增加和精神病的严重程度呈反比关系。
考虑到该疾病的临床表现中精神病性(嫉妒妄想、迫害妄想)和烦躁障碍的比例很高,治疗采用各种阻断多巴胺受体(吩噻嗪和丁酰苯衍生物)或降低组织中多巴胺水平(利血平)的神经安定剂。
建议使用氟哌啶醇(2-20毫克/天)、泰必利(100-600毫克/天),疗程不超过三个月;硫利达嗪(最高100毫克/天)、利血平(0.25-2毫克/天)以及抗惊厥药氯硝西泮(1.5-6毫克/天)。这些药物有助于减少运动过度,缓解情绪紧张,并弥补人格障碍。
精神障碍的住院治疗会根据患者的主诉症状、年龄和一般状况进行。门诊治疗的治疗原则相同(运动障碍的持续维持治疗,定期换药)。门诊治疗使用较低剂量的抗精神病药物。
轻度和中度痴呆症的康复措施包括职业治疗、心理治疗和认知训练。有必要与家属合作,并为患者的照护者提供心理支持。预防疾病的主要方法是对患者的近亲进行医学和遗传咨询,并在决定生育时推荐进行DNA分析。
预后一般不良,病程缓慢进展,多在10~15年后导致死亡。
 [ 18 ]
[ 18 ]
你有什麼煩惱?
亨廷顿氏病的治疗
亨廷顿病的治疗以对症治疗为主。舞蹈症和躁动可通过抗精神病药物(例如,氯丙嗪25-300毫克,口服,每日3次;氟哌啶醇5-45毫克,口服,每日2次)或利血平0.1毫克,口服,每日1次)部分抑制。剂量应增加至最大耐受剂量(直至出现嗜睡、帕金森综合征等副作用;利血平则需控制低血压)。经验性治疗的目标是减少经N甲基-O-天冬氨酸受体的谷氨酸能传递,并维持线粒体的能量产生。旨在增加脑内GABA水平的治疗无效。
基因检测和咨询至关重要,因为该疾病的症状通常在育龄期后才会出现。有家族病史或有意进行基因检测的人会被转诊至专门的医疗中心,并会充分考虑所有伦理和心理方面的影响。
亨廷顿氏病的对症治疗
目前尚无有效疗法能够阻止亨廷顿舞蹈症的进展。已开展了多项针对多种药物的试验,但均未取得显著疗效。神经安定剂和其他多巴胺受体拮抗剂被广泛用于纠正亨廷顿舞蹈症患者的精神障碍和不自主运动。不自主运动反映了多巴胺能系统和γ-氨基丁酸能系统之间的失衡。因此,神经安定剂用于降低多巴胺能活性过高。然而,这些药物本身可能引起严重的认知和锥体外系副作用。此外,除非患者出现精神病或躁动,否则其有效性尚未得到证实。神经安定剂常常会导致或加重吞咽困难或其他运动障碍。利培酮、氯氮平和奥氮平等新一代神经安定剂可能对亨廷顿舞蹈症的治疗特别有效,因为它们引起的锥体外系副作用较少,但可以减轻偏执症状或易怒情绪。
丁苯那嗪和利血平也会降低多巴胺能系统的活性,并可能在疾病早期减轻不自主运动的严重程度。然而,这些药物可能会引发抑郁症。由于该疾病本身常常会导致抑郁症,这种副作用极大地限制了利血平和丁苯那嗪的使用。在疾病晚期,携带多巴胺受体的细胞会死亡,因此多巴胺受体拮抗剂的疗效会减弱或丧失。
神经安定药、抗抑郁药和抗焦虑药可用于治疗亨廷顿舞蹈症患者的精神病、抑郁症和易怒症状,但这些药物只能在患者确实存在这些症状时才可使用。在疾病的某个阶段可能有效的药物,可能会随着病情的进展而变得无效,甚至有害。
GABA 受体激动剂已在亨廷顿氏病患者中进行了测试,因为亨廷顿氏病已被证实会导致纹状体中 GABA 水平显著下降,并且其投射区 GABA 受体高度敏感。苯二氮卓类药物已被证明可有效治疗因压力和焦虑而加重不自主运动和认知障碍的病例。应开具低剂量此类药物,以避免产生不必要的镇静作用。对于大多数亨廷顿氏病患者,这些药物均未显著改善其生活质量。
对于伴有帕金森病症状的早发性亨廷顿病患者,可以尝试使用多巴胺能药物,但其疗效有限。此外,左旋多巴可能引起或加重这些患者的肌阵挛。同时,巴氯芬可能减轻部分亨廷顿病患者的肌强直。
 [ 26 ], [ 27 ], [ 28 ], [ 29 ]
[ 26 ], [ 27 ], [ 28 ], [ 29 ]
亨廷顿氏病的预防性(神经保护性)治疗
尽管亨廷顿氏病的基因缺陷已为人所知,但它导致选择性神经元变性的原因仍不清楚。有人推测,旨在减少氧化应激和兴奋性毒性的预防性疗法可能能够减缓或阻止疾病进展。这种情况可能与肝豆状核变性有些相似,肝豆状核变性中的基因缺陷多年来一直不为人知,但针对其次级效应——铜积累——的预防性疗法却被“治愈”。在这方面,亨廷顿氏病与能量代谢紊乱和兴奋性毒性导致的细胞死亡相关的假说引起了特别的关注。该疾病本身可能由于亨廷顿蛋白N端片段的核内聚集而导致细胞死亡,从而破坏细胞和代谢功能。由于某些神经元群对兴奋性毒性损伤的敏感性更高,这一过程可能比其他神经元群受到更大的影响。在这种情况下,使用兴奋性氨基酸受体拮抗剂或预防自由基损伤的药物进行预防性治疗将能够预防或延缓疾病的发生和进展。在肌萎缩侧索硬化症的实验室模型中,抗氧化剂和受体拮抗剂 (RAA) 已被证明能够减缓疾病的进展。类似的方法可能对亨廷顿氏病有效。目前,谷氨酸受体拮抗剂和增强线粒体电子传递链复合物 II 功能的药物的临床试验正在进行中。
 [ 30 ]、[ 31 ]、[ 32 ]、[ 33 ]、[ 34 ]、[ 35 ]、[ 36 ]、[ 37 ]、[ 38 ]、[ 39 ]
[ 30 ]、[ 31 ]、[ 32 ]、[ 33 ]、[ 34 ]、[ 35 ]、[ 36 ]、[ 37 ]、[ 38 ]、[ 39 ]


