慢性息肉病性鼻炎
該文的醫學專家
最近審查:29.06.2025
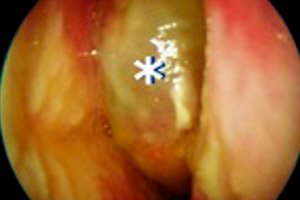
炎症过程伴随鼻腔和鼻窦内息肉的形成和复发性生长,提示慢性鼻窦炎伴鼻息肉 (CRSwNP)。尽管采取了保守治疗和手术治疗,息肉仍会反复出现。病理过程会扩散至微循环床和分泌性腺体结构。息肉生长主要由浸润中性粒细胞和嗜酸性粒细胞的水肿性组织形成。其他淋巴结样结构也参与了这一反应。治疗措施复杂,旨在改善患者的生活质量并预防复发。
流行病學
具有临床表现的慢性息肉性鼻窦炎的患病率为 1-5%。慢性鼻息肉性鼻窦炎 (CRSwNP) 是一种中年疾病,平均发病年龄为 42 岁,典型的诊断年龄为 40-60 岁。[ 1 ] 据统计,这种病症在欧洲人口中的患病率为 2-4%,但亚临床病程的发病率要高得多,估计约占总人群的 30%。
2015年,Stevens及其同事对在三级医疗中心接受鼻窦手术的慢性鼻窦炎(CRSwNP)患者进行了一项研究,发现患有慢性鼻窦炎(CRSwNP)的女性比男性病情更严重。[ 2 ] 关于儿童发病率的统计数据相对较少。已知10岁以下儿童患慢性息肉性鼻窦炎的几率远低于青少年和成年患者。据一些资料显示,儿童中鼻息肉的发病率不超过0.1%。
女性患者发病率较低,中年男性患者更易出现这种病症。
患者就诊时最常见的疾病症状是鼻塞。
原因 慢性息肉病性鼻炎
慢性息肉性鼻窦炎是指多因素疾病,尚无统一的病因学说。然而,当病变过程仅影响鼻窦黏膜组织,或合并囊性纤维化、支气管哮喘、卡塔格纳综合征、非甾体类抗炎药不耐受等疾病时,其病理机制可能存在局部性和全身性。遗传性息肉性鼻窦炎的发病率不能排除。
过敏症在伴有鼻息肉的慢性鼻窦炎 (CRSwNP) 中的作用一直是众多研究的焦点。尽管患有过敏性鼻炎和鼻息肉的患者比例与普通人群(0.5-4.5%)1 相似,但 51%-86% 的伴有鼻息肉的慢性鼻窦炎 (CRSwNP) 患者至少对一种空气过敏原致敏。[ 3 ] 迄今为止,尚无研究证实对某种特定空气过敏原的致敏与伴有鼻息肉的慢性鼻窦炎 (CRSwNP) 的发展之间存在关联,但在过敏季节,鼻窦疾病可能会恶化。[ 4 ]
哮喘与伴有鼻息肉的慢性鼻窦炎 (CRSwNP) 之间的关联已被更详细地定义。绝大多数哮喘患者(约 88%)至少有一些鼻窦炎症的放射学证据。更具体地说,据估计,所有哮喘患者中 7% 患有伴有鼻息肉的慢性鼻窦炎 (CRSwNP),而伴有鼻息肉的慢性鼻窦炎 (CRSwNP) 患者中 26%-48% 报告患有哮喘。[ 5 ]
组织学上,鼻腔息肉由病变的、通常为化生的上皮(位于增厚的基底膜上)和肿胀的基质(包含部分腺体和血管,但缺乏神经末梢)组成。典型的息肉基质以构成支撑基底的成纤维细胞、假囊肿和细胞成分(主要为嗜酸性粒细胞)为特征,这些成分位于腺体和血管附近以及覆盖的上皮组织下方。
推测在反复感染引起的增生形成初期,由于细胞内液体运输障碍,粘膜组织出现永久性肿胀。随着时间的推移,基底上皮膜破裂、脱垂并形成肉芽。
風險因素
影响粘膜组织炎症过程的形成和慢性息肉性鼻窦炎发生的因素:
- 内部因素:
- 遗传倾向;
- 男性,中年;
- 存在支气管哮喘;
- 对非甾体抗炎药不耐受;
- 花生四烯酸代谢失败;
- 免疫缺陷状态;
- 维生素 D 缺乏症;
- 代谢紊乱,肥胖;
- 阻塞性睡眠呼吸暂停综合征;
- 胃食管反流;
- 鼻腔解剖异常。
- 外部因素:
- 传染性病理学;
- 细菌携带者(如葡萄球菌);
- 病毒、冠状病毒感染,包括短暂性感染;
- 真菌病;
- 过敏原(药物、植物、工业等);
- 职业因素(多尘的房间、接触化学品、金属、霉菌或铁锈、经常接触动物或毒药等)。
發病
目前,关于慢性息肉性鼻窦炎的发病机制已知以下假设:
- 嗜酸性粒细胞炎症过程。嗜酸性粒细胞在息肉性鼻窦炎的炎症反应发展中起着重要作用。已知息肉组织中白细胞介素-5、嗜酸性粒细胞阳离子蛋白、嗜酸细胞趋化因子和白蛋白的存在增加。所有这些成分都会激活嗜酸性粒细胞的迁移,延长细胞凋亡,从而导致嗜酸性粒细胞炎症反应的发生。该过程的确切触发机制尚不清楚。
- IgE依赖性过敏反应(该理论为理论,尚未得到证实)。慢性息肉性鼻窦炎患者易发生花粉过敏和过敏性鼻炎。
- 白细胞介素 (IL)-17A 是一种主要由 Th17 细胞产生的细胞因子,在过敏反应、炎症和自身免疫的发展中起着至关重要的作用。[ 6 ],[ 7 ],[ 8 ],[ 9 ]
- 花生四烯酸代谢紊乱。水杨酸盐抑制环氧合酶,激活花生四烯酸的替代代谢途径,在5-脂氧合酶的作用下,花生四烯酸转化为白三烯。花生四烯酸的分解产物具有强效促炎介质的作用:它们能够诱发嗜酸性粒细胞迁移至呼吸道粘膜组织,从而加速炎症反应的发生。
- 细菌参与。细菌病原体在慢性息肉性鼻窦炎发展中的作用目前正在积极研究中。已知每两个患者中就有一个存在针对金黄色葡萄球菌外毒素的特异性IgE。感染性病原体可能参与了致病机制,但并非作为常见的过敏原,而是作为支持嗜酸性粒细胞炎症反应的强效抗原。金黄色葡萄球菌肠毒素被认为是息肉形成和进一步生长的原因,甚至可能与支气管哮喘同时发生。特异性“中性粒细胞”生长和化脓性息肉性鼻窦炎的检测也表明存在细菌。
- 真菌入侵。菌丝体颗粒在呼吸系统中普遍存在,因此在健康人群和易患息肉性鼻窦炎的患者中均有发现。在后者中,嗜酸性粒细胞被激活,在T淋巴细胞的影响下迁移到鼻窦中的粘液分泌物中。嗜酸性粒细胞攻击真菌颗粒,释放毒性蛋白质,导致鼻窦腔内形成浓稠的粘蛋白,损伤粘膜组织,引发炎症反应,进而导致息肉生长。据推测,菌丝体颗粒可以触发并维持易患该疾病人群的鼻窦炎症和息肉生长。然而,这一理论尚未得到充分证实。
- 急性呼吸道感染。有临床证据表明,即使在所谓的稳定缓解期,病毒也常常促使息肉再次出现并密集生长。
- 遗传易感性。息肉的发生与卡塔格纳综合征和囊性纤维化等遗传性疾病之间存在明确的联系,这为该理论提供了佐证。科学家们尚未确定导致该疾病形成的特定基因,因此相关研究成果较少。
- 鼻窦本身的病理(存在额外的鼻窦腔、囊性肿瘤等)。
局部息肉性鼻窦炎的病因包括各种解剖缺陷(鼻中隔偏曲、鼻甲结构不规则或钩状突起),这些缺陷都可能导致气道传导障碍。当主气流方向改变时,相应的黏膜组织区域会受到定期刺激。空气中的细菌、病毒和抗原会促使受损区域发生改变,引发细胞浸润,导致鼻孔道增生和阻塞。
由于慢性息肉性鼻窦炎是一种多病因疾病,因此不排除各种生物异常(无论是先天性的还是后天性的,存在于整个身体或单个器官、细胞或亚细胞结构中)的病理影响。因此,某些因素可能会导致自主神经系统紊乱,尤其是副交感神经系统过度活跃。疾病的易感性可能在接触任何诱发因素(例如感染、过敏原、机械损伤、化学损伤等)之前才会显现。
阑尾窦的慢性化脓性炎症反应被认为是一种独立的发病机制。慢性息肉性鼻窦炎在此成为继发性病变,主要发生在存在化脓性炎症的鼻窦中。至于弥漫性病变,则伴有逐渐蔓延至所有阑尾窦黏膜组织的现象。这类疾病属于全身性疾病,与免疫防御功能受损和全身反应性功能低下有关。
症狀 慢性息肉病性鼻炎
慢性息肉性鼻窦炎通常表现为两种或两种以上症状,其中最主要的症状是鼻塞和鼻腔呼吸困难。其他症状包括流鼻涕、面部疼痛(患侧鼻窦凸起处有压迫感)、嗅觉障碍,且持续时间超过12周。由此可见,上述症状并不具有特异性,即使没有鼻息肉,慢性鼻窦炎也可能出现。因此,通过鼻窦CT扫描和/或鼻内镜检查进行诊断至关重要。
因空气动力学异常而患上息肉性鼻窦炎的患者会抱怨鼻腔呼吸困难。检查过程中,可能会发现阻塞一侧鼻腔的息肉,或鼻中隔偏曲伴鼻壳结构不规则。患者可能无鼻涕分泌物。
真菌性慢性息肉性鼻窦炎的首发症状包括头痛。单侧或双侧鼻窦均可能受累。息肉的形成有时类似于肉芽肿,细菌感染也会出现这种症状。常伴有骨膜炎。
花生四烯酸代谢障碍患者的鼻息肉外观有所不同,形成实性息肉黏液肿块(化脓性炎症时,息肉结构更致密)。阑尾窦内充满粘稠、拖拽性的分泌物,难以与窦壁分离。
通常,当赘生物长大并离开鼻窦时,就会出现首发症状。患者会出现剧烈的鼻塞,使用血管收缩剂也无法缓解。平均而言,患有慢性鼻窦炎 (CRSwNP) 的患者比患有不伴鼻息肉的慢性鼻窦炎 (CRSsNP) 的患者有更严重的鼻窦症状。[ 10 ],[ 11 ] 在 126 名 CRS 患者队列中,Banjeri 及其同事发现鼻塞和嗅觉减退/嗅觉丧失与 CRSwNP 更显著相关,而面部疼痛/压迫感在 CRSsNP 患者中更常见。[ 12 ] 在选定的三级医疗中心对 CRS 患者进行的额外研究发现,与 CRSsNP 患者相比,CRSwNP 患者更容易报告流鼻涕、严重鼻塞和嗅觉/味觉丧失。 [ 13 ], [ 14 ]
其他病理特征包括:
- 经常头痛;
- 对气味的敏感性受损或丧失;
- 粘液和/或脓液排出;
- 鼻腔内有异物感;
- 呼吸问题,有时吞咽问题;
- 睡眠障碍,烦躁。
CT 和鼻窦内窥镜检查结果更差,表明患有不伴有鼻息肉的慢性鼻窦患者鼻旁窦受累平均比患有不伴有鼻息肉的慢性鼻窦患者更广泛。[ 15 ] 即使在接受鼻旁窦手术后,患有不伴有鼻息肉的慢性鼻窦患者鼻窦疾病的客观指标可能仍然比同样接受手术的患有不伴有鼻息肉的慢性鼻窦患者更差。[ 16 ]
儿童息肉性鼻窦炎
在幼儿(10岁以下)中,慢性息肉性鼻窦炎的发病率远低于成人(占所有儿童的不到0.1%)。儿童鼻息肉的发病机制尚不清楚。据推测,肿瘤是由慢性炎症过程、遗传性疾病引起的,并伴有呼吸系统黏膜组织的病变。我们经常谈论的是囊性纤维化,以及原发性纤毛运动障碍综合征。
息肉性鼻窦炎与过敏性疾病之间存在一定的关联。因此,在儿童中,超过30%的病例同时存在这两种疾病。
儿童慢性息肉性鼻窦炎的临床表现与成人基本相同。然而,专家指出,儿童息肉会更明显地降低生活质量,并对其他相关疾病的预后产生负面影响。
儿科的主要症状是鼻塞,并且通常会加重。
儿童期最常见的病例为上颌后孔息肉,占70%-75%。较大的单发肿块较少被诊断出来。
階段
为了客观评估慢性息肉性鼻窦炎的程度,采用Lund-Kennedy分期标准:
- 0-未见息肉;
- 1 息肉病局限于中鼻道;
- 2 - 息肉延伸到中鼻壳下边界之外,进入鼻腔。
还评估了粘膜肿胀的程度:
- 0-无肿胀;
- 1-轻微、中度水肿;
- 2-存在息肉组织变化。
存在异常放电:
- 0-无排放;
- 1-粘液分泌物;
- 2 - 分泌物浓稠(致密)和/或化脓。
形式
慢性鼻窦炎通常分为无息肉型和息肉型鼻窦炎。目前,尚无对慢性息肉型鼻窦炎的统一分类。但专家们会根据其临床和组织学特征以及病理原因,将该疾病分为不同的类型。
根据息肉的组织结构,区分:
- 过敏性息肉性鼻窦炎(又名水肿性、嗜酸性);
- 息肉囊性鼻窦炎,纤维化炎症,中性粒细胞;
- 腺性鼻窦炎;
- 伴有基质异型性的鼻窦炎。
根据病因病机特点,本病分类如下:
- 因鼻窦及鼻腔空气动力学障碍引起的息肉病;
- 息肉性化脓性鼻窦炎是在鼻腔和鼻窦慢性化脓性炎症过程的背景下发展起来的;
- 真菌性息肉病;
- 花生四烯酸代谢障碍引起的鼻窦炎;
- 囊性纤维化引起的息肉病、卡塔格纳综合征。
大多数专家认为,慢性息肉性鼻窦炎不是一个单一的疾病单位,而是一种包括多种病理状况的综合征,从任何鼻窦的局部病变到弥漫性病变,在支气管哮喘、非甾体抗炎药不耐受、遗传性疾病的背景下发现。
另外强调:
- 弥漫性双侧慢性息肉性鼻窦炎(特征是鼻腔和所有鼻窦中息肉的生长逐渐加重);
- 单侧、孤立性疾病(特别是筛后鼻孔、腭后鼻孔、蝶后鼻孔鼻窦炎)。
並發症和後果
最常见的并发症包括频繁流鼻血、慢性流鼻涕、嗅觉减退或丧失。此外,还经常发生继发感染,增加化脓性菌群的风险,从而导致鼻腔化脓性炎症的发生。在复杂病例中,不排除出现脓毒症的可能性。
息肉本身不会对患者的生命构成威胁,但会严重影响患者的生活质量。鼻腔和鼻窦中的息肉是各种微生物滋生和积累的理想场所,导致频繁的细菌感染、鼻出血、扁桃体炎、鼻炎、鼻窦炎、气管炎和喉炎,以及其他可能病程复杂的疾病。
鼻息肉由于持续存在的慢性炎症而十分危险。息肉生长会妨碍正常的呼吸功能和粘液分泌。因此,会导致以下问题:
- 阻塞性睡眠呼吸暂停(睡眠期间中断、屏住呼吸);
- 支气管哮喘复发;
- 鼻腔和鼻窦经常感染。
为了避免不良后果,必须及时咨询医生,接受所有必要的诊断和治疗。
診斷 慢性息肉病性鼻炎
诊断措施始于收集患者主诉、病史以及进行客观检查。获取的信息用于确定进一步的诊断策略。
专家澄清:
- 最初症状出现的时间(鼻呼吸困难、异常分泌物、头痛、嗅觉障碍);
- 如果有鼻窦炎病史;
- 是否对耳鼻喉器官进行过任何外科手术干预;
- 患者是否接受过任何治疗(其他医生开的处方或自我治疗)。
必须查明息肉病的遗传易感性,并回顾病史。应特别注意是否存在遗传性疾病、支气管哮喘、内分泌疾病和不良习惯。
然后,医生会进行前后鼻镜检查,即鼻腔内镜检查。检查时需关注鼻腔结构的解剖结构、黏膜组织和鼻孔复合体的状态。息肉性鼻窦炎通常会在鼻腔内或鼻腔外、鼻腔和/或鼻咽部发现息肉。此外,还会检查黏膜肿胀情况,以及是否存在黏液或脓性分泌物。明确息肉的发展阶段至关重要。
组织学分析是强制性的。典型的息肉病增生表现为:受损的、通常为化生的上皮组织位于致密的基底膜上,以及水肿性基质,基质中腺体数量少,血管网络稀疏,神经末梢数量极少。基质内存在成纤维细胞(支撑框架的基础),以及细胞成分和假囊肿。主要存在的细胞是中性粒细胞和嗜酸性粒细胞,位于血管和腺体附近,或位于上皮组织正下方。[ 17 ]
仪器诊断首先包括放射学检查,特别是鼻窦的计算机断层扫描。CT扫描可以了解炎症反应的强度,并检测解剖特征。如果要进行手术,那么专家需要掌握关于介入部位的全面信息,以防止术后并发症的发生。医生会使用X射线详细检查上颌窦、额窦、楔窦以及格子迷路的前部和后部。病情评估采用以下评分标准:
- 0-存在窦气化;
- 1-气化作用部分降低;
- 2-气化总量减少。
此外,还需评估两侧鼻孔复合体的状况:
- 0-无病理变化;
- 2-鼻孔复合体未定义。
完全性弥漫性息肉性鼻窦炎患者的最高总分为 24 分。
鑑別診斷
当儿童和老年患者发现鼻息肉时,应特别注意排除以下情况:
- 在儿童时期 - 如果是双侧病理过程则为囊性纤维化,如果是单侧过程则为脑膨出;
- 在老年患者中 - 其他良性和恶性肿瘤,这在单侧病变或非典型定位中尤其重要。
息肉性鼻窦炎和支气管哮喘的结合代表了最复杂的疾病表型之一,难以为患者的诊断和治疗管理提供建议。
对于所有寻求医疗帮助的患者,都会收集其详细的生活史和疾病史,以及强制性的过敏病史。
在所有病例中,均需对以下类型的肿瘤进行鉴别诊断:
- 内翻性乳头状瘤是一种有恶性变性的可能上皮性肿瘤。
- 鳞状细胞癌是鼻窦中最常见的恶性肿瘤。
- 黑色素瘤是由鼻腔或鼻窦黑色素细胞构成的恶性肿瘤。
- 嗅神经母细胞瘤是一种由嗅觉神经上皮发展而来的罕见肿瘤。
- 血管外皮细胞瘤是一种在颅底发育的血管肿瘤。
- 鼻胶质瘤是一种罕见的神经胶质组织良性肿瘤。40%的病例为鼻内胶质瘤。
- 青少年鼻咽血管纤维瘤是一种罕见的良性血管肿瘤,类似于息肉。
对于单侧病理改变,应排除所有可能的良、恶性肿瘤。任何肿瘤都可能与慢性息肉性鼻窦炎相似或共存。所有手术切除的息肉组织均应进行组织形态学检查,以排除恶性肿瘤和化生的可能性,并进一步制定合理的治疗方案。
誰聯繫?
治療 慢性息肉病性鼻炎
治疗措施包括温和手术、延长吸入性糖皮质激素疗程以及短期全身性皮质激素治疗。部分患者需接受抗真菌治疗和抗生素治疗。
患有鼻息肉的慢性鼻窦炎 (CRSwNP) 患者的医疗治疗选择仍然有限。根据美国最近的指南,建议将局部皮质类固醇和生理盐水鼻腔冲洗作为患者的初始医疗治疗。[ 18 ] 经鼻皮质类固醇可以缩小鼻息肉的大小,减轻鼻窦症状,并改善患者的生活质量。[ 19 ],[ 20 ] 口服皮质类固醇也可以缩小息肉的大小并改善症状,但鉴于其与严重的全身副作用有关,应始终谨慎使用。[ 21 ] 抗生素可能有助于治疗患有鼻息肉的慢性鼻窦炎 (CRSwNP) 的感染性加重,但大型随机试验缺乏具有临床显著疗效(即息肉减少)的结果。
药物治疗包括使用以下药物组和治疗类型:
- 局部用糖皮质激素(鼻腔给药)有助于缩小息肉,预防手术切除后早期复发。副作用通常仅限于鼻腔干燥和流鼻血。对晶状体状态和眼压没有影响。常用药物包括莫米松、氟替卡松、环索奈德,较少使用布地奈德、倍氯米松、倍他米松、地塞米松、曲安奈德。标准剂量为200-800微克。
- 对于鼻窦手术后复发性慢性息肉性鼻窦炎患者,可将皮质类固醇植入物植入格状迷路。该手术可改善鼻腔通畅度,延长缓解期。最常见的是可自吸收的植入物,释放370微克糠酸莫米松。植入物的作用持续时间为1个月。
- 短期皮质类固醇疗程(1至3周)包括口服甲泼尼龙,剂量为每公斤体重1毫克,并在2-3周内逐渐减量。这种方法可以减轻临床症状,改善鼻窦状况。治疗通常与抗生素疗法或吸入皮质类固醇联合使用。治疗示例:口服泼尼松龙,剂量为每日0.5-1毫克/公斤体重,持续10-15天。从第8天开始逐渐减量,每日减量5毫克,直至完全停药。对于慢性息肉性鼻窦炎,最佳疗程为每年1-2个疗程。
- 使用生理性氯化钠溶液或林格氏溶液冲洗鼻腔,通常添加透明质酸钠、木糖醇和木葡聚糖,也能显示出积极的治疗效果。
- 如有指征,可开具短期或长期全身性抗生素治疗(副作用:肠功能障碍、厌食)。需注意的是,低剂量大环内酯类药物具有免疫调节作用,可维持稳定的术后缓解。开具长期疗程时,应考虑大环内酯类药物可能产生的心脏毒性。
- 局部用抗菌药物用于冲洗鼻腔。例如,莫匹罗星溶液的疗效与口服阿莫西林/克拉维酸钾相似,后者已成功用于对抗金黄色葡萄球菌。
- 抗组胺药物适用于治疗伴有过敏症状的患者。
囊性鼻窦炎和息肉性鼻窦炎禁用物理治疗。
息肉性鼻窦炎的生物疗法
如果慢性息肉性鼻窦炎的病程无法控制,则可在主要治疗的基础上加用单克隆抗体生物疗法。对于已接受鼻窦手术的双侧病变患者,如果满足以下三项标准,则可使用单克隆抗体治疗息肉性鼻窦炎;对于未接受手术或无法接受手术的患者,如果满足以下四项标准,则可使用单克隆抗体治疗:
生物治疗标准 |
标准指标 |
T2炎症过程的临床表现。 需要全身性皮质类固醇治疗或存在禁忌症。 对生活质量产生明显的负面影响。 嗅觉功能明显恶化。 与支气管哮喘合并。 |
视野内(x400)组织嗜酸性粒细胞大于10,或血液嗜酸性粒细胞大于250kL/μL,或总IgE大于100IU/mL。 每年两个以上疗程,或长期小剂量治疗。 SNOT-22 量表得分为 40 分或以上。 嗅觉丧失。 支气管哮喘需要定期接受皮质类固醇吸入治疗。 |
生物治疗的效果应在治疗开始后4个月和1年后进行评估。如果根据上述标准(至少其中一项)未获得积极疗效,则应停止治疗。
评估结果的标准:
- 息肉体积缩小;
- 减少全身使用皮质类固醇药物的需要;
- 改善嗅觉功能;
- 总体上提高生活质量;
- 减少背景病理的影响。
如果对以上所有标准均有积极回应,则生物治疗指标为优秀;如果对三到四项标准有积极回应,则生物治疗指标为中等。对1-2项标准有积极回应则评估为弱。
迄今为止,已有多种单克隆抗体被用作治疗药物,特别是度匹鲁单抗[ 22 ]、奥马珠单抗、美泊利单抗[ 23 ]、贝那利珠单抗和瑞利珠单抗。基于度匹鲁单抗的皮下注射液——用于治疗息肉性鼻窦炎的Dupixent通常是首选药物。[ 24 ] 成人初始推荐剂量为每两周300毫克。如果漏注射,应尽快注射,然后按照先前开具的方案继续注射。
度匹鲁单抗 |
每两周皮下注射300毫克一次。12个月后,可改为每四周一次给药。 |
奥马珠单抗 |
开始时,每 2 至 4 周皮下注射 75 至 600 毫克一次。 |
美泊利单抗 |
每月一次,皮下注射100毫克。 |
草药治疗
官方医学不赞成在慢性息肉性鼻窦炎患者中使用民间疗法,因为这会增加病情恶化和息肉生长强度的风险。只有在咨询主治医生并结合医生开出的主要治疗方案后,才允许使用民间疗法。
可能的植物疗法食谱:
- 将5汤匙南瓜籽与200毫升沙棘油研磨均匀。每日一次,餐前15分钟服用1茶匙。服用频率:服用10天,停药5天,直至病情稳定好转。本品应冷藏保存。
- 将等量的洋甘菊和白屈菜混合。取1汤匙混合物倒入200毫升沸水中,盖上盖子静置数小时。每次餐前30分钟服用1汤匙。疗程为4周,之后可休息10天后再次服用。
- 将1汤匙杜松子放入锅中,倒入200毫升沸水,小火煮10分钟。待药液冷却后过滤,每日三次,每次50毫升,饭后一小时服用。
手术治疗
外科手术干预包括功能性内窥镜手术,以切除息肉、纠正解剖缺陷(鼻中隔偏曲、鼻壳肥大等)、检查和纠正鼻窦腔的大小、打开和切除受病理生长影响的格子迷路细胞。
息肉切除遵循微创手术原则,尽量减少对黏膜组织的损伤。手术时保留鼻中隔,并保留其支撑功能。如发现上颌窦有其他连接,则将其与主窦连接。
如果是息肉性化脓性鼻窦炎,干预措施包括恢复鼻腔连通,为鼻窦的正常气体交换创造条件,去除肿块和脓液。在这种情况下,即使存在水肿,也不会切除鼻窦的粘膜组织。在进行手术之前,医生会查明炎症过程的微生物学特征,确定病原体的类型及其对抗菌药物的敏感性。
真菌性息肉性鼻窦炎也采用类似的方法。在这种情况下,有时需要通过前壁或下鼻道进行微创鼻窦切开术。清除鼻窦内真菌感染的主要条件是恢复通气。
对于囊性纤维化患者,卡塔格纳综合征息肉需要定期切除,因为在所有情况下都会重新生长。
預防
慢性息肉性鼻窦炎尚无特异性预防方法。建议避免危险因素的影响,定期就医进行预防性检查,并及时治疗任何耳鼻喉科疾病。
已患息肉的患者应尽一切努力预防息肉复发。医生会根据个人情况安排就诊,包括定期检查鼻腔、清除分泌物和积聚物,以及使用抗菌药物进行局部治疗。长期局部治疗建议使用皮质类固醇。如果患者接受过手术治疗,则应每三个月就诊一次。如果鼻窦曾有化脓性或真菌性病变,则应至少每六个月就诊一次。
如果慢性息肉性鼻窦炎合并支气管哮喘或对非甾体类抗炎药不耐受,则需长期(数年或终身)经鼻使用皮质类固醇。如果药物无法阻止息肉生长,则需反复干预,防止息肉过度生长并阻塞鼻腔呼吸。
在良好的情况下,皮质类固醇治疗可以在夏季暂时停止,并在初秋恢复,这与息肉重新生长的高风险有关。
預測
治疗的主要目标是延长疾病的无症状期并改善患者的生活质量。大多数患者必须接受反复和多次内镜手术,每日经鼻给予局部皮质类固醇(通常终生,定期)。
耳鼻喉科医生会每2-3个月对患者进行系统性监测。治疗预后不仅取决于手术方案、主治医生的资质,还取决于患者对医疗建议的依从性。
需要注意的是,切除鼻息肉并不能消除其出现的根本原因,因此一段时间后,息肉可能会再次出现。为了降低复发的可能性,必须遵医嘱,并在手术后进行长期药物治疗。
息肉性鼻窦炎和军队
如果应征入伍者被诊断患有鼻息肉和鼻窦息肉,则可将其划分为以下资格类别:
- 适合服兵役;
- 受限制的。
如果慢性息肉性鼻窦炎被正式确诊,包括CT扫描,则可能受到服务限制。此外,入伍时,患者必须在药房登记至少六个月。
如果应征士兵接受了手术切除肿瘤,并且没有复发,且对健康没有危害,则被划归为“适合服兵役”类别。
如果有文件证据表明肿瘤定期复发、呼吸问题,如果出现鼻窦炎并发症,那么我们可以谈论健身限制,较少的情况下 - 关于不适合服役。
在大多数情况下,急性期的慢性息肉性鼻窦炎成为推迟动员和义务服务的指征。


